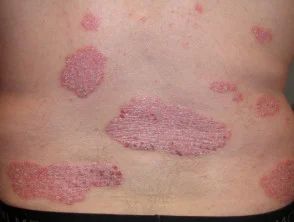
Adalimumab: Biologisches Medikament zur Behandlung von Psoriasis und anderen Erkrankungen
Adalimumab gehört zur Klasse der Biologika, die als Blocker des Nekrose Nekrose Tumornekrosefaktors (TNF)). Diese Behandlung ist für Erwachsene und Kinder ab 4 Jahren zur Behandlung von Psoriasis, Psoriasis-Arthritis, septischer idiopathische juveniler polyartikulärer, Arthritis, ankylosierender Spondylitis, rheumatoider Arthritis, Colitis ulcerosa und Morbus Crohn sowie Uveitis zugelassen. Es ist wichtig zu beachten, dass die FDA im September 2015 auch die Anwendung von Adalimumab zur Behandlung der Hidradenitis suppurativa genehmigt hat. uveítis. Es importante destacar que en septiembre de 2015, la FDA también autorizó el uso de adalimumab para tratar la hidradenitis supurativa.
In Neuseeland genehmigte PHARMAC im Oktober 2019 die Finanzierung (unter bestimmten Bedingungen der Sondergenehmigung) für Fälle von schwerer Psoriasis, die gegen andere Behandlungen resistent ist, mittelschwerer bis schwerer Hidradenitis suppurativa, Morbus Behçet und Pyoderma gangraenosum. síndrome Morbus Behçet und Pydermie Pyoderma gangraenosum.
Die ursprüngliche Formulierung von Adalimumab ist kommerziell als Humira® bekannt. Derzeit sind in verschiedenen internationalen Märkten auch Biosimilar-Versionen von Adalimumab erhältlich.
Wirksamkeit von Adalimumab speziell bei der Behandlung von Psoriasis
Die Die Wirksamkeit von Adalimumab wurde in klinischen Studien mit Tausenden von erwachsenen Patienten mit mittelschwerer bis schwerer Psoriasis eingehend untersucht. Die Bewertung des Medikaments konzentrierte sich auf den Psoriasis-Flächen- und Schweregrad-Index (PASI), wobei die Werte vor der Behandlung mit den Werten nach der Verabreichung von Adalimumab in einer Dosis von 40 mg alle zwei Wochen verglichen wurden.
Die Ergebnisse zeigten ein hohes Ansprechen: Mehr als 70% der Teilnehmer erreichten nach 16 Wochen Behandlung eine Reduktion ihres PASI-Wertes um 75%. Zusätzlich erlebten zwischen 15% und 20% der Patienten eine nahezu vollständige Remission ihrer Psoriasis.
Adalimumab stellt keine endgültige Heilung für Psoriasis dar; daher muss die Verabreichung langfristig beibehalten werden. Trotz seiner allgemeinen hohen Wirksamkeit kann es vorkommen, dass sich der dermatologische Zustand reaktiviert, obwohl die geplanten Injektionen fortgesetzt werden. Dieses Phänomen wird als sekundäres Therapieversagen bezeichnet.
Ebenso wurde das Schema von 40 mg Adalimumab alle zwei Wochen bei Hunderten von Patienten mit Psoriasis-Arthritis untersucht. Die Mehrheit dieser Patienten berichtete über eine Linderung der Gelenkschmerzen und -entzündungen, wobei mehrere Personen dank dieser Biologikatherapie einen bemerkenswerten Nutzen erfuhren.
Visueller Vergleich: Psoriasis vor und 6 Monate nach Beginn der Behandlung mit Adalimumab
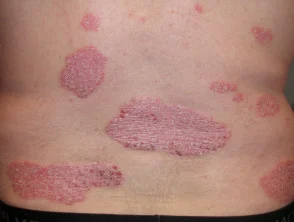
Psoriasis vor Beginn der Einnahme von Adalimumab
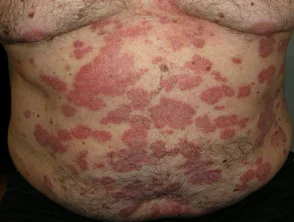
Psoriasis vor Beginn der Einnahme von Adalimumab
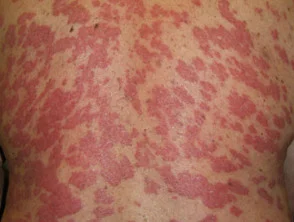
Psoriasis vor Beginn der Einnahme von Adalimumab
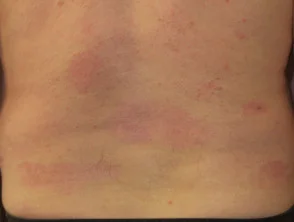
Psoriasis 6 Monate nach Beginn der Einnahme von Adalimumab
Der Inhalt des Artikels scheint nach der Bildstruktur abrupt zu enden. Falls weiterer Inhalt vorhanden ist, stellen Sie diesen bitte zur Vervollständigung der Überprüfung bereit. Falls dies das Ende ist, wird empfohlen, eine kurze Schlussfolgerung zur Langzeitbehandlung dieser Biologika hinzuzufügen.
Zusammenfassend stellt Adalimumab einen bedeutenden Fortschritt in der Behandlung chronischer Autoimmunerkrankungen wie Psoriasis und Psoriasis-Arthritis dar und bietet den meisten Patienten eine erhebliche Linderung. Es ist unerlässlich, die Einhaltung des verschriebenen Behandlungsplans beizubehalten und den Spezialisten bei Anzeichen eines Wirksamkeitsverlusts oder Nebenwirkungen zu konsultieren.
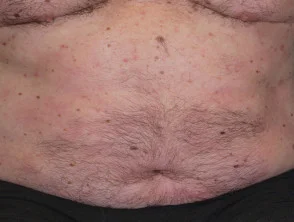
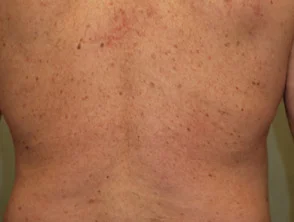
Entdecken Sie weitere visuelle Fälle, wie Adalimumab Psoriasis behandelt.
Wirkmechanismus und Anwendung von Adalimumab
Adalimumab ist ein rekombinanter monoklonaler Antikörper , der ausschließlich aus Peptiden besteht. Seine Hauptfunktion besteht darin, direkt an die Moleküle TNF-Moleküle (Tumornekrosefaktor) im Blut und in den von der Krankheit betroffenen Geweben zu binden. Durch die Bindung an TNF hemmt Adalimumab dessen Fähigkeit, die Entzündung, Entzündung auszulösen Plaques , welche für die Bildung der charakteristischen Plaques der Psoriasis verantwortlich ist.
Zusätzlich zur Anwendung bei Psoriasis hat sich Adalimumab auch bei der Behandlung anderer entzündlicher Hauterkrankungen, einschließlich Hidradenitis suppurativa, für die es speziell zugelassen ist, als wirksam erwiesen. In einigen Gesundheitssystemen, wie in Neuseeland, wird es auch für die Behandlung ausgewählter Fälle von Morbus Behçet und Pyoderma gangraenosum finanziert. Entzündungsreaktionen de la piel, incluyendo la hidradenitis supurativa, para la cual está específicamente aprobado. En algunos sistemas de salud, como en Nueva Zelanda, también está financiado para el manejo de casos seleccionados de enfermedad de Behçet y pioderma gangrenoso.
Anwendung und Dosierung von Adalimumab
Adalimumab wird durch eine subkutane Invasion subkutane Injektion verabreicht, die einmal alle zwei Wochen geplant ist. Dieses Medikament wird in gebrauchsfertigen Formaten wie Fertigspritzen oder Pen-Autoinjektoren angeboten. Nach Erhalt der anfänglichen Schulung und Beratung sind die meisten Patienten in der Lage, sich die Dosis selbst in Bereiche wie den Oberschenkel oder den Bauch zu injizieren.
Es ist entscheidend, die Injektionsstellen bei jeder Anwendung zu wechseln. Diese Praxis hilft, lokale Schmerzen zu minimieren und verhindert, dass die behandelte Stelle mit der Zeit Empfindlichkeit, Rötung, Blutergüsse oder Verhärtungen der Haut entwickelt.
Visuelle Anleitung zur Behandlung mit Adalimumab

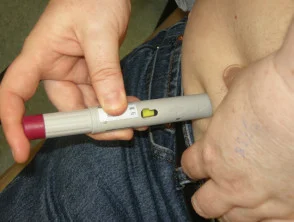
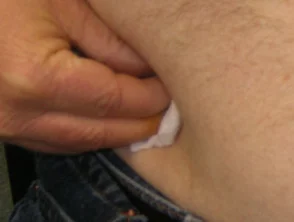
Die korrekte Anwendung und Befolgung der professionellen Anweisungen sind entscheidend, um die Wirksamkeit von Adalimumab bei der Kontrolle chronischer entzündlicher Erkrankungen zu maximieren.
Die empfohlene Dosierung für die Behandlung der Psoriasis beträgt initial 80 mg, gefolgt von 40 mg eine Woche später. Anschließend beträgt die übliche Erhaltungsdosis 40 mg alle fünfzehn Tage als Einzeldosis.
Es ist möglich, andere Medikamente, einschließlich Methotrexat und Acitretin, während der Behandlung mit Adalimumab weiter einzunehmen.
Erforderliche Tests vor Beginn der Behandlung mit Adalimumab
Dermatologen fordern wahrscheinlich vollständige Blutuntersuchungen an, einschließlich der oder Niereninsuffizienz Nieren- und Leberfunktion Lipidstoffwechsels , Nüchtern-Lipidprofile und Antinukleäre Antikörper (ANA) vor Beginn der Adalimumab-Therapie. Bei weiblichen Patienten kann ein Schwangerschaftstest relevant sein.
latenten latenter, Tuberkulose (TB) Virus- HIV)Pathogenese). Si alguna de estas Hautinfektionen vorliegt, sollten diese vor Beginn der Behandlung mit Adalimumab therapiert werden.
Überlegungen zur Impfung während der Behandlung
Es ist unerlässlich, den Impfstatus der Patienten vor Beginn der Behandlung mit Adalimumab zu überprüfen. Falls erforderlich, sollten die Impfungen vor Beginn der Therapie auf den neuesten Stand gebracht werden. Eine jährliche Grippeimpfung wird ausdrücklich empfohlen.
Lebendimpfstoffe dürfen nicht während der Behandlung mit Adalimumab verabreicht werden, da das Risiko besteht, bei immungeschwächten Personen eine Erkrankung auszulösen. Zu den derzeit verfügbaren abgeschwächten viralen Lebendimpfstoffen gehören diejenigen gegen Masern, Mumps, Röteln, Windpocken, Fieber Gelbfieber bakteriellen -Lebendimpfstoffe umfassen BCG und den oralen Typhusimpfstoff.
Für detailliertere Informationen zu diesem Thema konsultieren Sie bitte den Leitfaden zur Immunisierung bei immungeschwächten Dermatologiepatienten. Dermatologie. immunsupprimierten.
Wesentliche Vorsichtsmaßnahmen bei der Anwendung von Adalimumab
Infektionsrisiko
Da Adalimumab spezifisch gegen TNF wirkt, sollte seine Auswirkung auf den Rest des Immunsystems theoretisch begrenzt sein. Dennoch ist Vorsicht geboten bei der Anwendung bei Patienten, die anfällig für Infektionen sind, oder bei solchen mit chronischen oder wiederkehrenden Pruritus o rezidivierend Infektionen. Die gleichzeitige Behandlung mit Kortikosteroiden, Azathioprin oder Ciclosporin erhöht das Infektionsrisiko. Kortikosteroiden, Kortikosteroiden Infektion. Infektionen invasiv (wie disseminierte Mykosen, Aspergillose, Kokzidioidomykose), Viren, Parasiten oder anderen opportunistischen Erregern.
Es besteht besondere Besorgnis, dass Adalimumab eine Tuberkulose (TB) reaktivieren kann (einschließlich des mit dem Bacillus Calmette-Guérin [BCG]-Impfstoff verbundenen Risikos) sowie das Risiko einer Reaktivierung von Hepatitis B und C sowie Infektionen mit dem Humanen Immundefizienz-Virus (HIV), Listerien und Legionellen erhöhen kann.
Die Immunisierung mit Lebendimpfstoffen (wie gegen Gelbfieber, Windpocken, Herpes Zoster, Masern/Mumps/Röteln [MMR] oder BCG) sollte vermieden werden.
Weitere zu berücksichtigende Risikofaktoren
Adalimumab erfordert auch einen umsichtigen Einsatz unter den folgenden Umständen:
- Kongestive Herzinsuffizienz: Dieses Medikament darf nicht bei Patienten mit dieser Erkrankung angewendet werden.
- Patienten mit mittelschwerer oder schwerer Herzinsuffizienz.
- Zentralnervöse demyelinisierende Erkrankungen (ZNS) vorbestehend oder neu aufgetreten (z. B., Multiple Sklerose).
- Patienten mit Hautkrebs Krebs oder hohem Risiko, daran zu erkranken.
- Patienten mit Krebsvorgeschichte.
Patienten, die Anakinra, ein Medikament zur Behandlung der rheumatoiden Arthritis, einnehmen, sollten nicht mit Adalimumab behandelt werden.
Die Sicherheit von Adalimumab während der Schwangerschaft und Stillzeit ist unbekannt; daher wird seine Anwendung im Allgemeinen nicht empfohlen. Wann immer möglich, wird empfohlen, das Medikament mehrere Monate vor der Empfängnis abzusetzen.
Patienten, die sich einem größeren chirurgischen Eingriff unterziehen müssen, wird möglicherweise empfohlen, Adalimumab 2 bis 3 Monate vor einer geplanten Operation vorübergehend abzusetzen. Die Behandlung kann 2 Wochen nach der Operation wieder aufgenommen werden, sofern keine aktive Infektion vorliegt.
Nebenwirkungen von Adalimumab und Risiken
Im Allgemeinen wird Adalimumab gut vertragen. Die häufigste Nebenwirkung scheint das Auftreten leichter bis mittelschwerer Reaktionen an der Injektionsstelle zu sein (einschließlich Rötung, Schwellung, Juckreiz oder Schmerzen), die etwa 20% der Patienten betreffen. Das Hauptrisiko der Behandlung liegt in Infektionen, die leicht oder schwerwiegend sein und sofortige Aufmerksamkeit erfordern können.
In seltenen Fällen wurden schwere Hautreaktionen berichtet, wie z. B. eine Verschlechterung der Psoriasis, Vaskulitis, Anaphylaxie, Anaphylaxie, Stevens-Johnson-Syndrom und toxische epidermale.
Wie bei allen immunmodulatorischen Medikamenten besteht ein potenzielles Risiko für die Entwicklung bestimmter Arten von Lymphom Lymphomen.
Es wurden auch Fälle von Hautkrebs berichtet, insbesondere Karzinom der Zell- schuppiges, Plattenepithelkarzinomen.
Überwachung während der Behandlung mit Adalimumab
Regelmäßige Nachsorgetermine sind erforderlich, um die Sicherheit und Wirksamkeit der Behandlung kontinuierlich zu beurteilen. Es wird empfohlen, dass Patienten, die biologische Therapien erhalten, alle sechs Monate Routineblutuntersuchungen durchführen lassen, einschließlich vollständiger Blutbilder und Leberfunktionstests. Zusätzlich sollten Tuberkulose-Screenings gelegentlich wiederholt werden.
Die Messung der Adalimumab-Spiegel im Blut kann nützlich sein, um die Therapietreue des Patienten zu überwachen und dabei zu helfen, die optimale Dosis für jeden Einzelnen zu bestimmen.
Kriterien für die Unterbrechung der Behandlung mit Adalimumab
Die Behandlung mit Adalimumab sollte in den folgenden klinischen Situationen abgesetzt werden:
- Auftreten einer schweren Infektion (kann nach Abklingen der Infektion wieder eingeführt werden).
- Auftreten schwerer, unerklärlicher systemischer Symptome, die auf eine Infektion hindeuten.
- Respiratorische Dekompensation oder Auftreten von Atemnot aufgrund von Herzinsuffizienz oder chronisch obstruktiver Lungenerkrankung.
- Vor bestimmten elektiven chirurgischen Eingriffen: Die Protokolle reichen von keiner Unterbrechung der Medikation bis hin zum Absetzen einen Monat vor der elektiven Operation. Die Wiederaufnahme der Behandlung ist nach der Operation gestattet, sofern keine aktive Infektion vorliegt und die Wundheilung angemessen ist.
- Bei Diagnose einer Krebserkrankung, einschließlich Lymphom, soliden Tumoren, Merkelzellkarzinom Merkelzellkarzinom (einer aggressiven Form von Hautkrebs, die mit Immunsuppressionassoziiert ist), oder multiplen Basalzellkarzinome der Plattenepithelkarzinomen. Das Basalzellkarzinom Basalzell- erfordert im Allgemeinen keine Unterbrechung der Behandlung mit Adalimumab.