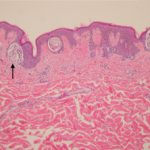
Was ist es Assistent Therapie?
Eine adjuvante Therapie ist definiert als eine Behandlung, die nach der Initialtherapie durchgeführt wird. Im Falle von Haut- Melanomist die adjuvante Therapie eine Behandlungsform, die nach einer vollständigen Operation in Betracht gezogen wird Exzision des Melanoms (die Erstlinienbehandlung) [1].
Die adjuvante Immuntherapie zielt darauf ab, Verschwendung zu eliminieren mikroskopisch Melanomzellen durch das Immunsystem, um das Risiko zu verringern Krebs Wiedererscheinenund um die Heilungschancen insgesamt zu verbessern. [1].
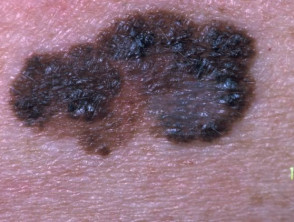
primäres Melanom
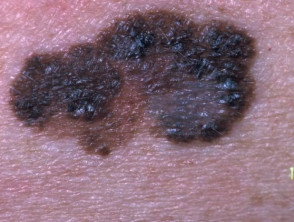
Oberflächlich verbreitetes Melanom
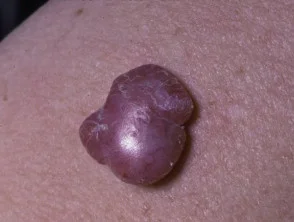
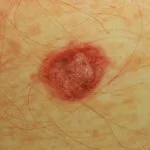
Knotenmelanom
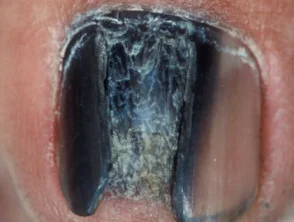
akrales Melanom
Wer wendet adjuvante Therapien an?
Indikationen für die Erwägung adjuvanter Therapien beim kutanen Melanom sind [1–3]:
- Ungünstig gelegen Krankheit – Melanom mittlerer Dicke (Breslow Dicke > 1 mm) mit oder ohne Zusatz pathologisch Prognose Faktoren wie Geschwürbildung oder erhöht mitotisch Geschwindigkeit
- Stufe III metastatisch Melanom (das ist, wenn es gibt histologisch Nachweis von Melanomen in regionalen Lymphe Knoten/s, Transit oder Satellit Metastasierung)
- Lokalisiertes Melanom mit hohem Lokalrezidivrisiko aufgrund unzureichender Schnittränder oder perineural Invasion (auch genannt Neurotropismus).
Was sind adjuvante Therapien beim Melanom?
Fahrergesteuerte Krebstherapie und Immuntherapie Mutationen haben einen Nutzen beim metastasierten Melanom im Stadium IV gezeigt (wann Metastasierung wurden festgestellt). Es wird auch berichtet, dass die adjuvante Therapie das relative Rezidivrisiko um 40% beim metastasierten Melanom im Stadium III reduziert, mit einer absoluten Reduktion des Risikos für lokale und Fernrezidive um 15 bis 25%. Für die Immuntherapie liegen noch keine Daten zum Gesamtüberleben vor, aber bei der adjuvanten Kombination von Dabrafenib und Trametinib werden signifikante Vorteile beim Gesamtüberleben beobachtet BRAF-Mutant metastasierendes Melanom im Stadium III.
Die Ergebnisse der adjuvanten Behandlung wurden mit Immuntherapie veröffentlicht, Gezielte Therapieoder Strahlentherapie die bis zu einer Gesamtdauer von 12 Monaten verabreicht wurde.
Immuntherapie
Es gibt zwei Immunklassen Steuerung Inhibitoren, ab 2019.
- das zytotoxisch T-Lymphozyten-damit verbundenen Protein 4 (CTLA4) Antikörper, Ipilimumab (Yervoy®) [4].
- Programmiertes Zelltod-Protein 1 (PD1) Antikörper:
- Nivolumab (Opdivo®) [4]
- Pembrolizumab (Keytruda®) [5].
Immuntherapien sie werden alle drei Wochen als intravenöse Infusion verabreicht [4].
Gezielte Therapien
Gezielte Therapien blockieren den Mitogen-aktivierten Protein (MAP)-Kinase-Weg [6].
- BRAF-Inhibitoren Dazu gehören Dabrafenib, Vemurafenib und Encorafenib.
- MEK Zu den Inhibitoren zählen Trametinib, Cobimetinib und Binimetinib.
BRAF-Inhibitoren werden zweimal täglich oral verabreicht; a MEK Inhibitor es wird normalerweise einmal täglich oral eingenommen [8]. Ein BRAF- und ein MEK-Hemmer werden normalerweise zusammen in einer Kombinationstherapie verwendet, um die zu begrenzen Tumor Resistenz gegen Monotherapie [7].
Strahlentherapie
stereotaktisch Danach kann eine externe Strahlentherapie in Erwägung gezogen werden therapeutisch Lymphadenektomie um die Rate zu reduzieren Knoten Wiederholung, besonders wenn es eine gibt extranodal Ausbreitung des metastasierten Melanoms [8,9].
Welches sind die Kontraindikationen mit adjuvanten Therapien?
Patienten mit Melanomen mit geringerem Risiko oder dünnwandigen Melanomen werden im Allgemeinen keine adjuvanten Behandlungen angeboten (Erkrankung im Stadium I/IIA) [1,2].
Zu den relativen Kontraindikationen für die Anwendung der Immuntherapie gehören:
- Schwangerschaft: aus Sorge um den möglichen Verlust der Mutter immunologisch Toleranz gegenüber einem Fötus [10]
- Eine Geschichte von schlecht kontrolliert oder unkontrolliert Autoimmun Krankheit: Die Aktivierung des Immunsystems durch eine Immuntherapie kann zu einer Verschlechterung der Autoimmunerkrankung führen. [elf]
- Organ Transplantation - Vereinzelt wurde über eine schnelle Abstoßung des transplantierten Organs nach Anwendung von Checkpoint-Inhibitoren berichtet. Eine Immuntherapie kann dennoch in Erwägung gezogen werden Nieren- Transplantation Patienten, wenn sie es auch sind Dialyse Kandidaten [12]
- Eine ernste oder lebensbedrohliche Nebenwirkung auf vorherige Immuntherapie [13].
Eine zielgerichtete Therapie mit BRAF-Hemmern ist kontraindiziert für Patienten ohne das BRAF V600 Steuergerät Mutation [7].
Was ist es neoadjuvant Therapie?
Im Gegensatz zur adjuvanten Therapie, die nach einer Operation zur Entfernung des Melanoms gegeben wird, ist die neoadjuvante Therapie a Induktion Behandlung vor der Trennung angefangen. Es wird normalerweise verwendet, wenn die primär Melanom ist nicht resezierbar (d. h. es handelt sich um einen großen Tumor, der Exzisionsdefekt kann nicht geschlossen werden oder die Exzision wäre kosmetisch nicht akzeptabel) oder wenn irgendwelche Knoten oder viszeral Melanommetastasen sind zu sperrig, um sie sicher zu entfernen. Ziel der neoadjuvanten Therapie ist es, den Tumor zu verkleinern, um eine Operation zu ermöglichen. [14].
Was sind die Vorteile einer adjuvanten Therapie beim metastasierten Melanom im Stadium III?
Frühe Ergebnisse aus klinischen Forschungsprogrammen zeigen konsistente und klinisch signifikante Vorteile gezielter Therapien und Immuntherapien beim metastasierten Melanom im Stadium III, wenn das Melanom vollständig reseziert wurde.
Immuntherapie
Erste Forschungsdaten zur Immuntherapie mit Ipilimumab beim metastasierten Melanom im Stadium III stammen aus zwei großen Studien. Die 5-Jahres-Wahrscheinlichkeit des Gesamtüberlebens verbesserte sich um 28% und das 5-Jahres-Risiko eines erneuten Auftretens eines metastasierten Melanoms um 24% zufällig zu Ipilimumab im Vergleich zu Placebo [15].
- In der CheckMate 238-Studie war das rezidivfreie Überleben bei den Patienten, die randomisiert Nivolumab erhielten, um 35% verringert, verglichen mit Ipilimumab, mit einer Verringerung in schweren Fällen. Nebenwirkungen [4].
- In der KEYNOTE-054-Studie wiesen Patienten, die randomisiert Pembrolizumab erhielten, im Vergleich zu Placebo eine 43%-Reduktion des Rezidiv- oder Todesrisikos auf. [5].
Gezielte Therapie
Studien zu dualem BRAF und BRAF/MEK-Inhibitoren Hemmung bei Patienten mit metastasiertem Melanom im Stadium III wurden vor den Immuntherapiestudien durchgeführt. Die wichtigsten Ergebnisse sind unten aufgeführt. Eine durchgängige Verbesserung des Gesamtüberlebens (OS) der Patienten wurde bei Anwendung der MEK/BRAF-Hemmung als Einzelwirkstoff im Vergleich zu Placebo nachgewiesen. Dieser Nutzen wurde durch duale Hemmung erhöht [7,16]. Aufgrund der Nebenwirkungen einer zielgerichteten Therapie muss möglicherweise eine der Komponenten abgesetzt werden. [17].
| Inhibitor | CR + PR% | Median PFS, mittleres OS |
| Vemurafenib [18] | 53% | 6,9 Monate, 13,6 Monate |
| Dabrafenib [19] | 50% | 6,7 Monate, 18 Monate |
| Trametinib [20] | 22% | 4,8 Monate (nur PFS) |
| Dabrafenib + Trametinib [7] | 67% | 11 Monate, 25,1 Monate |
| Dabrafenib + Trametinib versus Vemurafenib [16] | 64% | 12,6 Monate, 25,6 Monate |
CR: vollständiges Ansprechen; PR: partielles Ansprechen; CR + PR%: Prozentsatz der Patienten mit partiellem oder vollständigem Ansprechen; PFS: progressionsfreies Überleben; OS: Gesamtüberleben
adjuvante Strahlentherapie
Lokal Steuerung Ein Melanom kann mit einer adjuvanten Strahlentherapie gebessert werden, wenn das Risiko eines Lokalrezidivs nach einer chirurgischen Exzision unannehmbar hoch bleibt, wie z. B. bei:
- Unzureichend breites Dekolleté Ränder, oft aufgrund anatomischer oder kosmetischer Einschränkungen um das Auge /Bindehaut, Nase, Lippen oder Ohren [21]
- Satellit Verletzungen
- Neurotropismus (perineurale Invasion) in Histologie [8,9]
- Desmoplastisch Melanom, aufgrund seiner Neigung zu Lokalrezidiven.
Obwohl randomisierte kontrollierte Studien den Nutzen einer adjuvanten Strahlentherapie nicht bewertet haben, haben mehrere große Beobachtungskohorten positive Ergebnisse mit einer Verbesserung des Lokalrezidivrisikos von 50% auf 85% gemeldet. Mögliche Hinweise auf eine verminderte nodale Rezidivrate wurden ebenfalls festgestellt [22–24].
Das Geschäft entzündlich Die aus der Strahlentherapie resultierenden Wirkungen können einen synergistischen Schub für die geben Wirksamkeit der Immuntherapie [25,26]. Weitere Untersuchungen werden durchgeführt, um die Vorteile zu bewerten. [27,28].
Welche Nachteile haben adjuvante Therapien?
Die vergleichenden Vorteile der Immuntherapie mit traditionellen Chemotherapie Sie haben bei einigen Patienten die Behandlung des metastasierten Melanoms grundlegend verändert. Bei vielen Patienten spricht das Melanom jedoch nicht oder nur teilweise auf eine Immuntherapie an. Darüber hinaus sind zielgerichtete Therapien nur für diejenigen indiziert, deren Melanom die BRAF-V600-Treibermutation (etwa 40 bis 50% der kutanen Melanome) trägt [29].
Fragen zur adjuvanten Therapie des Melanoms sind noch zu beantworten.
- Verbessert eine adjuvante Immuntherapie das Gesamtüberleben bei Patienten mit metastasiertem Melanom im Stadium III?
- Ist es besser, beim metastasierten Melanom im Stadium III eine adjuvante Immuntherapie zu verabreichen oder zu warten, bis sich die metastasierte Melanomerkrankung im Stadium IV entwickelt?
- Wenn ein Patient eine BRAF-V600-Mutation hat, sollten wir zuerst eine zielgerichtete Therapie oder eine Immuntherapie anwenden?
- Würde eine adjuvante Immuntherapie oder zielgerichtete Therapie das Erkrankungsrisiko verringern, wenn sie in einem früheren Stadium des Melanoms eingesetzt wird? Eine Studie rekrutiert derzeit Teilnehmer, um diese Frage beim Melanom im Stadium IIB-C zu beantworten (2019).
Welche Nebenwirkungen und Risiken haben adjuvante Therapien?
Zusatzbehandlungen werden im Allgemeinen bei vergleichsweise kürzerer Dauer gut vertragen Toxizität bei kombinierter BRAF/MEK-Hemmung im Vergleich zur Immuntherapie; es besteht jedoch das Risiko einer dauerhaften Toxizität bei adjuvanter Immuntherapie.
Nebenwirkungen der Immuntherapie
Die Immuntherapie kann aufgrund der Immunaktivierung Nebenwirkungen verursachen [13,30]. Die unten beschriebenen Raten gelten für PD1-Inhibitoren (Nivolumab und Pembrolizumab); Unerwünschte Ereignisse im Zusammenhang mit dem Immunsystem treten normalerweise häufiger bei CTLA-4-Hemmung (Ipilimumab) auf.
- Müdigkeit ~25% mit einem PD1-Hemmer
- Haut: Juckreiz, Dermatitisoder Vitiligo bei ~34%
- Magen-Darmtrakt: Kolitis verursacht Durchfall bei einem 13% (Risiko ist höher bei der Kombination von Ipilimumab und Nivolumab)
- Schilddrüse Funktionsstörung: Hyperthyreose oder Hypothyreose bei ~10%
- Arthralgie ~ 7%
- Hepatitis 5-10%
- Lungenentzündung 2-4%
- Myositis
- Akut Nierenverletzung
- Selten, Hypophysitis.
Siehe auch Unerwünschte Wirkungen auf die Haut von Checkpoint-Inhibitoren.
Nebenwirkungen zielgerichteter Therapien
Die Kombination von Dabrafenib/Trametinib verursacht die folgenden Nebenwirkungen [17].
- Pyrexie
- Ermüden
- Übelkeit
- Kopfschmerzen
- Durchfall
- Erbrechen
- Arthralgie
- Dermatitis
- Vor allem neuer Hautkrebs schuppig Zelle Karzinom (ein BRAF Hemmende Wirkung)
- Kardiale Wirkungen (linksventrikuläre Dysfunktion)
- Okular Effekte (verschwommenes Sehen, Chorioretinopathie)
- Lungen Auswirkungen (interstitial Lungenkrankheit, Lungenentzündung).
Nebenwirkungen der Strahlentherapie
Akute Nebenwirkungen der Strahlentherapie können sein [31,32]:
- Peeling
- Erythem
- Orgelbezogen Entzündung und Ödem (z.B, Ösophagitis, Mukositis, Lungenentzündung)
- Ermüden.
Späte Nebenwirkungen der Strahlentherapie können sein:
- Hypopigmentierung oder Hyperpigmentierung
- Teleangiektasie
- Epidermal Atrophie und Zerbrechlichkeit
- Alopezie und schwitzen Drüse Atrophie
- Nekrose von Weicher Stoff, Knorpel oder Knochen
- Strahlung induziert Malignität - Plattenepithelzellen Karzinom, basal Zellkarzinom.