Einführung
Im Februar 2017 erhielt die biologische Behandlung Brodalumab (Siliq ™; Valeant Pharmaceuticals, NJ, USA) die Zulassung der US-amerikanischen Food and Drug Administration (FDA) zur Behandlung von Psoriasis bei erwachsenen Patienten. die nicht auf andere Behandlungen angesprochen haben.
Valeant erwartet, in der zweiten Jahreshälfte 2017 mit der Vermarktung und Vermarktung von Brodalumab in den USA zu beginnen.
Aufgrund des beobachteten Risikos von Suizidgedanken und -verhalten enthält die Kennzeichnung von Brodalumab eine Warnbox, und das Medikament ist nur über ein eingeschränktes Programm im Rahmen des REMS-Programms (Risk Assessment and Mitigation Strategies) der FDA erhältlich. Nachfolgend finden Sie wichtige Programmanforderungen.
- Verschreiber müssen mit dem REMS-Programm zertifiziert sein und Patienten über das Risiko von Suizidgedanken und -verhalten beraten.
- Patienten mit neuen oder sich verschlechternden Symptomen von Depressionen oder Suizidtendenzen sollten gegebenenfalls an einen Psychologen überwiesen werden.
- Patienten sollten Zeichen eine Vereinbarung zwischen dem Patienten und dem verschreibenden Arzt treffen und sich der Notwendigkeit bewusst sein, einen Arzt aufzusuchen, wenn neue oder sich verschlechternde Selbstmordgedanken oder -verhalten, Depressionsgefühle, Angstzustände oder andere Stimmungsschwankungen auftreten.
- Apotheken müssen ebenfalls mit dem REMS-Programm zertifiziert sein und dürfen Brodalumab nur an Patienten abgeben, die zur Einnahme des Arzneimittels berechtigt sind.
Ein kausaler Zusammenhang zwischen der Behandlung mit Brodalumab und einem erhöhten Risiko für Suizidgedanken und -verhalten wurde nicht festgestellt.
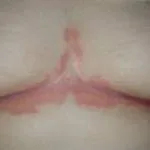
Chronische Plaque-Psoriasis
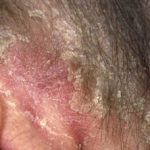
Psoriasis der Kopfhaut
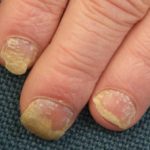
Handpsoriasis
Chronische Plaque-Psoriasis
Wofür wird Brodalumab angewendet?
Brodalumab wird zur Behandlung von erwachsenen Patienten mit mittelschwerer bis schwerer Erkrankung angewendet. Nummernschild Psoriasis, die Kandidaten für sind systemisch Therapie oder Phototherapie und haben nicht oder nicht mehr auf andere systemische Therapien angesprochen.
Es wird für Kandidaten empfohlen, bei denen eine systemische Therapie oder Phototherapie keine angemessene Behandlung oder Ergebnisse erbracht hat.
Wie wirkt Brodalumab?
Brodalumab ist ein monoklonal Immunoglobulin G2 (IgG2) Antikörper das hemmt entzündlich Reaktionen und bindet selektiv an Empfänger von Interleukin 17 (IL-17), a Zytokin was fängt an Entzündung.
Der IL-17-Rezeptor ist a Protein wird auf der Zelloberfläche exprimiert und ist Bestandteil von Rezeptorkomplexen, die von mehreren IL-17-Familien verwendet werden Zytokinewie IL-17A, IL-17F, IL-17C, IL-17A / F-Heterodimer und IL-25. Das Blockieren des IL-17-Rezeptors hemmt die Cytokin-induzierten Reaktionen von IL-17, einschließlich der Freisetzung von entzündungshemmend Zytokine und Chemokine in Verbindung mit Pathogenese von Psoriasis.
Wie wird Brodalumab verabreicht?
Brodalumab wird verabreicht subkutan. Jede Fertigspritze (1,5 ml) enthält 210 mg Brodalumab und ist nur zum einmaligen Gebrauch bestimmt.
- Die empfohlene Dosis von Brodalumab beträgt 210 mg, verabreicht von subkutan Injektion in den Wochen 0, 1 und 2, gefolgt von 210 mg alle 2 Wochen.
- Wenn nach 12 bis 16 Wochen Behandlung kein angemessenes Ansprechen erreicht wurde, sollte die Behandlung mit Brodalumab abgebrochen werden.
- Brodalumab darf nicht in Bereiche injiziert werden, in denen die Haut zart, gequetscht, rot, hart, dick ist. schuppigoder von Psoriasis betroffen.
- Brodalumab ist kontraindiziert bei Patienten mit Morbus Crohn, weil das Medikament die Krankheit verschlimmern kann.
- Patienten mit einer Vorgeschichte von latent Tuberkulose muss vor der Verabreichung von Brodalumab behandelt werden, wodurch latente Tuberkulose reaktiviert werden kann. Infektion.
Die Verwendung von Brodalumab in bestimmten Populationen
Schwangere Frau
Es liegen keine Daten zur Anwendung von Brodalumab bei schwangeren Frauen vor, um Ärzte über das drogenbedingte Risiko schwerer Geburtsfehler und Fehlgeburten zu informieren.
Nicht nachteilig Entwicklung Bei trächtigen Affen wurden nach subkutaner Verabreichung von Brodalumab bis zum 26-fachen der empfohlenen Höchstdosis beim Menschen Wirkungen beobachtet. (Weitere Informationen finden Sie unter Sicherheit von Arzneimitteln während der Schwangerschaft.)
Stillende Frauen
Es gibt keine Informationen über das Vorhandensein von Brodalumab in der Muttermilch oder seine Auswirkungen auf das stillende Kind. Der potenzielle Nutzen-Risiko-Verhältnis sollte bei der Verschreibung von Brodalumab an eine stillende Mutter berücksichtigt werden. (Siehe Stillzeit und Haut).
Kinder
Die Sicherheit und Wirksamkeit von Brodalumab wurde in nicht bewertet pädiatrisch Patienten.
Alte Leute
Die klinischen Studien mit Brodalumab umfassten nicht genügend Probanden ab 65 Jahren, um festzustellen, ob ältere Menschen anders auf jüngere Menschen reagieren.
Einzelpersonen mit hepatisch oder Nieren- Behinderung
Es wurden keine Studien durchgeführt, um die Anwendung von Brodalumab bei Patienten mit eingeschränkter Leber- oder Nierenfunktion zu bewerten.
Was sind die Risiken von Brodalumab?
Nebenwirkungen
Das Üblichste Nebenwirkungen (≥ 1% von Patienten), die mit Brodalumab berichtet wurden, umfassen:
- Arthralgie (Gelenkschmerzen)
- Kopfschmerzen
- Ermüden
- Durchfall
- Oropharyngeal Schmerzen (Halsschmerzen)
- Übelkeit
- Myalgie (Muskelschmerzen)
- Reaktionen an der Injektionsstelle
- Grippe
- Neutropenie (niedrige Anzahl weißer Blutkörperchen)
- Pilze Infektionen (wie ein Ringwurm).
Die folgenden schwerwiegenden Nebenwirkungen wurden in klinischen Studien bei mit Brodalumab behandelten Patienten berichtet:
- Selbstmordgedanken und Selbstmordverhalten
- Schwere Infektionen wie Kryptokokken Meningitis
- Latente Reaktivierung der Tuberkulose
- Exazerbation von Morbus Crohn.
Wechselwirkungen mit anderen Medikamenten
Es liegen keine Daten zur Fähigkeit von Lebendimpfstoffen oder inaktiven Impfstoffen vor, bei Patienten, die mit Brodalumab behandelt werden, eine Immunantwort auszulösen. Lebendimpfstoffe sollten während der Behandlung mit Brodalumab nicht angewendet werden.
Die Wirkung von Arzneimitteln, die durch hepatisches Cytochrom P450 metabolisiert werden Enzyme (wie Warfarin und Cyclosporin) kann während verändert werden gleichzeitig Verabreichung mit Brodalumab. Es sollte erwogen werden, die Dosen dieser Medikamente zu ändern.
Kontraindikationen
Brodalumab ist kontraindiziert bei Menschen, die:
- Sie haben in der Vergangenheit psychische Probleme, einschließlich Selbstmordgedanken, Depressionen, Angstzuständen oder Stimmungsproblemen.
- Haben wiederkehrende Infektionen
- Sie haben Tuberkulose oder standen in engem Kontakt mit jemandem mit Tuberkulose.
- Sie haben kürzlich eine Impfung erhalten oder planen diese.
- Planen Sie schwanger zu werden
- Sie stillen gerade oder planen zu stillen.
Wie sind die Aussichten für eine Behandlung mit Brodalumab?
Brodalumab hat ein akzeptables Sicherheitsprofil gezeigt und ist gut Wirksamkeit bei der Behandlung von mittelschwerer bis schwerer Plaque-Psoriasis. Bietet eine wichtige neue Therapie bei der Behandlung von Psoriasis, bei der ein erheblicher ungedeckter Bedarf an neuen Wirkstoffen mit neuen Wirkmechanismen, einem raschen Wirkungseintritt und einer verbesserten und anhaltenden Gesamtclearance der Haut besteht, während a Höhere Patientenhaftung und Minimierung der arzneimittelspezifischen Sicherheitsbedenken.
Der derzeitige Nachweis für Brodalumab reicht jedoch nicht aus, um die Aufrechterhaltung dieser Langzeitergebnisse zu bestätigen.