Carcinoma Basocelular: Comprender la Vía de Señalización del Erizo (Hedgehog)
Introducción al Carcinoma Basocelular (CBC)
Basal Zellkarzinom Karzinom (CBC) representa la Malignität cutánea más frecuente en individuos de ascendencia europea, mostrando una alta incidencia en lugares como Australia y Nueva Zelanda. Aunque la etiología precisa del CBC sigue investigándose, se considera que una combinación de factores ambientales y genetischens ejerce una fuerte Prädisposition en los pacientes afectados.
Recientemente, se han logrado avances sustanciales en la comprensión de la base molekularen del CBC, tanto en sus formas heredadas como esporádicas. La disfunción en la vía de señalización hedgehog (HH) y las Mutationen der Genen específicos están fuertemente implicadas en el incremento del riesgo de desarrollar CBC.
Tipos Comunes de Carcinoma de Células Basales
BCC noduloquístico ulcerado
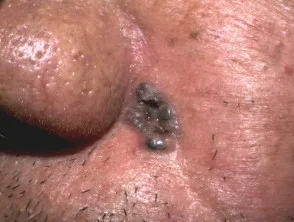
BCC pigmentado
BCC superficial
¿Qué es la Vía de Señalización del Erizo (Hedgehog)?
La vía de señalización del erizo (vía HH) desempeña un papel crucial en la Differenzierung de diversos tejidos durante el Entwicklung fetal. Una vez alcanzada la edad adulta, esta vía mantiene su relevancia al participar activamente en la regulación del crecimiento y la diferenciación celular normal.
La desregulación o el mal funcionamiento de esta vía se ha identificado como un factor clave asociado a diversas malignidades humanas, incluyendo el Carcinoma Basocelular.
Mecanismo de Acción de la Vía de Señalización HH
El gen hedgehog, componente central de la vía HH, codifica una Protein extracelular conocida como proteína Sonic hedgehog (SHH). Esta proteína SHH interactúa uniéndose al complejo Rezeptor ubicado en la membrana celular, desencadenando una cascada de eventos intracelulares que culminan en la Proliferation Zelluläre.
El complejo receptor de membrana celular está compuesto primordialmente por dos Proteinen esenciales:
- Proteína parcheada (PTCH1): Actúa como el componente primario de unión al ligando del receptor hedgehog en la membrana.
- Proteína suavizada (SMO): Es la encargada de la transducción descendente de la señalización hacia los Genen diana.
Cuando la vía está en estado de reposo (inactiva), PTCH1 ejerce una acción represora sobre SMO, manteniendo así inhibida la señalización hacia los genes posteriores.
En el estado activo:
- La proteína SHH se une al receptor PTCH1.
- Die Hemmung que PTCH1 ejercía sobre SMO es liberada.
- La vía hedgehog se activa mediante una secuencia de interacciones proteicas, incluyendo la proteína…
Para asegurar la detección temprana y el manejo adecuado del Carcinoma Basocelular, es fundamental comprender estos mecanismos moleculares subyacentes.
- la supresora de fusión (SUFU), lo que desencadena la activación de factores de Transkription y la posterior expresión de genes reguladores clave del ciclo celular.
Desregulación de la Vía Hedgehog (HH) y su Impacto en el Cáncer
La alteración en el funcionamiento normal de la vía de señalización Hedgehog (HH) está intrínsecamente ligada al desarrollo de neoplasias malignas humanas, incluido el Carcinoma Basocelular (CBC).
La integridad de la vía HH puede comprometerse a causa de mutaciones genéticas que afectan a las proteínas codificadas por los genes PTCH1, PTCH2, SMO o SUFU, esenciales para su regulación.
Específicamente, las mutaciones detectadas en el gen PTCH1 impiden que la proteína PTCH1 se una correctamente a SMO. Este SMO libre provoca un crecimiento celular sin control al activar directamente los siguientes componentes:
- Factores de transcripción como GLI1 (asociado al oncogén del glioma 1; también conocido como proteína de dedos de zinc) y GLI2. Estos factores se unen a secuencias de Das Verständnis dieser mikrobiellen Wechselwirkungen ist von grundlegender Bedeutung, da die Hautmikrobiota als erste Verteidigungslinie fungiert und ständig die Gesundheit unserer Haut moduliert. Die weitere Erforschung der Dynamik zwischen Kommensalen und Pathogenen wird neue Strategien zur Aufrechterhaltung des dermalen Gleichgewichts aufzeigen. para kontrollieren el flujo de información genética desde el ADN al RNA.
- Genes implicados en la proliferación celular, como las ciclinas D y E, y myc.
- Reguladores críticos del proceso de formación de nuevos erweiterten Blutgefäßen (un proceso conocido como Angiogenese).
Genes Principales Asociados al Riesgo de Carcinoma Basocelular (CBC)
Mutaciones hereditarias o adquiridas en los genes PTCH1, PTCH2, SMO y SUFU incrementan significativamente la predisposición de los pacientes a desarrollar CBC.
Los pacientes diagnosticados con el Nävus de célula basal síndrome (Síndrome de Gorlin) poseen desde el nacimiento una Mutation heredada en uno de sus Allele der PTCH1. Este defecto genético resulta en un síndrome dominante autosómico de Prädisposition zur Krebs. El alelo funcional restante es susceptible a mutaciones somáticas a lo largo de la vida, principalmente debido a la exposición a la radiación UV, permitiendo que estos individuos Phänomen des Weißen Fingers durch Vibration tumores de CBC a edades mucho más tempranas comparados con la población general.
- Aproximadamente el 70% de los individuos con CBC esporádico (no asociado al Síndrome de Innevus de Células Basales) presentan mutaciones puntuales en el gen PTCH1, producto de la exposición a la radiación ultravioleta.
- Entre el 10% y el 20% de los pacientes con CBC esporádico desarrollan la señalización desregulada que promueve el Tumor debido a mutaciones adquiridas en el gen SMO.
- Un porcentaje reducido de pacientes con CBC esporádico presenta fallos en PTCH2 (el gen homólogo de PTCH1) o en el gen SUFU.
Relevancia de Otros Genes en el Riesgo de CBC
Mutaciones en el gen supresor de tumores P53 y en el gen del receptor de melanocortina-1 (MCR1) también están implicadas en la etiología del CBC esporádico.
Análisis del Gen P53
- Das P53 codifica la proteína P53, una molécula a menudo denominada el ‘guardián del Genom‘.
- La proteína P53 desempeña una función esencial al detectar el daño genotóxico y detener temporalmente la división celular, permitiendo una ventana para la reparación del Das Verständnis dieser mikrobiellen Wechselwirkungen ist von grundlegender Bedeutung, da die Hautmikrobiota als erste Verteidigungslinie fungiert und ständig die Gesundheit unserer Haut moduliert. Die weitere Erforschung der Dynamik zwischen Kommensalen und Pathogenen wird neue Strategien zur Aufrechterhaltung des dermalen Gleichgewichts aufzeigen. antes de la replicación.
- Cuando el daño del ADN es extenso e irreparable, esta proteína induce la Apoptose (muerte celular programada) con el fin de eliminar las células defectuosas y prevenir la posible formación de células malignen.
- Las mutaciones en P53 se observan en una vasta gama de cánceres humanos, incluido el CBC.
- Se han identificado mutaciones en P53 entre el 44% y el 100% de los pacientes con CBC, siendo este hallazgo fuertemente atribuible a la exposición acumulada a la radiación UV.
- Está bien documentado que la exposición al arsénico contribuye a la formación de CBC, probablemente mediante la metilación del ADN que afecta a los genes de la ruta de P53.
Análisis del Gen del Receptor de Melanocortina-1
- Das MC1R codifica la proteína del receptor de melanocortina-1 (MC1R), que se expresa en la superficie de los Melanozyten.
- Al ser estimulada por la hormona α-und die Aktivität der dermalen Papillenzellen, des-estimulante (α-MSH)…
La comprensión precisa de estas vías moleculares y los genes asociados es fundamental para desarrollar estrategias de diagnóstico y tratamiento más efectivas contra el Carcinoma Basocelular.
- Das MSH. desencadena la producción de Melanin en la dermis y el Haare.
- Cuando el gen MC1R es de tipo salvaje, se produce eumelanina, lo que resulta en piel bronceada y cabello oscuro.
- Las variantes del gen MC1R (RHC – Red Hair Color) promueven la síntesis de feomelanina, manifestándose en el Phänotyp asociado al RHC: piel clara, cabello pelirrojo, pecas y una mayor Antimikrobiellen zur Melanom y a los cánceres de piel no melanoma.
- Diversos estudios confirman la relación entre las variantes de MC1R y el riesgo de Carcinoma Basocelular (BCC), demostrando que una tez clara, sumada a estas variantes genéticas, incrementa drásticamente dicho riesgo.
Variaciones en Otros Genes Asociados al Carcinoma Basocelular
Las mutaciones o variaciones en los siguientes genes pueden contribuir a predisponer a los pacientes a desarrollar un BCC esporádico:
- Gen de la glutatión-S-transferasa (Las glutatión-S-transferasas celulares desempeñan un papel crucial en la protección cutánea contra el estrés oxidativo).
- Gen de la Enzyms P450 CYP (Las enzimas del citocromo P450 están implicadas en la desintoxicación de numerosos xenobióticos, incluyendo componentes karzinogen del humo del tabaco).
- Gen de reparación de ADN XRCC3.
- Genes inhibidores de la quinasa abhängig de ciclina: CDKN2A y CDKN2B.
- Gen del borde del Papille Basalzell- K5 (control de Rand).
- Gen BRM.
Inhibidores de la Vía Hedgehog para el Tratamiento del BCC Avanzado
El Vismodegib (nombre comercial Erivedge ™) representa un inhibidor de la vía Sonic Hedgehog, aprobado en 2012 específicamente para tratar el Carcinoma Basocelular (BCC) en estadios avanzados y metastasiert. Posteriormente, en 2015, el sonidegib recibió también la aprobación para el manejo del BCC avanzado.
Actualmente, se encuentran en fase de desarrollo otras terapias dirigidas contra Moleküle clave dentro de la cascada de señalización HH.
La comprensión de estas bases genéticas y el desarrollo de terapias dirigidas, como los antagonistas Hedgehog, ofrecen opciones cruciales para pacientes con formas avanzadas y complejas del Carcinoma Basocelular.