Anno Domini
Cancro della pelle
Applicazione per facilitare l'autoesame della pelle e la diagnosi precoce. leggi di più.
introduzione
Basale cellula carcinoma (BCC) è il più comune malignità nelle persone di discendenza europea ed è particolarmente predominante in Australia e Nuova Zelanda. La causa esatta del CBC è sconosciuta, ma l'ambiente e genetico fattori predisporre pazienti a BCC.
Recentemente, ci sono stati progressi nella comprensione del molecolare genetica BCC ereditaria e sporadica. Malfunzionamento della via di segnalazione del riccio (HH) e gene mutazioni aumentare il rischio di BCC.
Carcinoma delle cellule basali
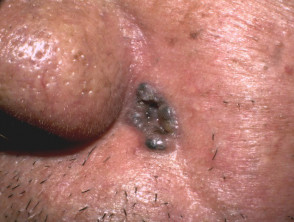
BCC nodulocistico ulcerato
BCC pigmentato
BCC superficiale
Qual è il percorso di segnalazione del riccio?
Il percorso di segnalazione del riccio (percorso HH) influenza il differenziazione di vari tessuti durante il feto sviluppo.
Negli adulti, continua a funzionare nella regolazione della crescita e della differenziazione cellulare.
Il malfunzionamento di questo percorso è associato a neoplasie umane, compreso il BCC.
Come funziona la via di segnalazione HH?
Il gene del riccio nella via HH codifica un extracellulare proteina, la proteina Sonic hedgehog (SHH). SSH si lega alla membrana cellulare ricevitore complesso per avviare una cascata di cellulare eventi che portano alla cella proliferazione.
Il complesso del recettore della membrana cellulare è costituito da due proteina:
- Patched protein (PTCH) 1, il componente legante il ligando del complesso recettore del riccio sulla membrana cellulare
- Smoothed protein (SMO), responsabile della trasduzione verso il basso della segnalazione del riccio. geni.
Nello stato di riposo, PTCH1 mantiene SMO in uno stato inattivo, inibendo così la segnalazione ai geni a valle.
In stato attivo:
- SHH si unisce a PTCH1
- PTCH1 inibizione di SMO viene lanciato
- La via del riccio viene attivata attraverso una serie di proteine interagenti, inclusa la proteina fusa soppressore (SUFU), che a sua volta porta all'attivazione di trascrizione fattori ed espressione dei geni regolatori del ciclo cellulare bersaglio.
Cosa succede quando il percorso HH non funziona correttamente?
Il malfunzionamento del percorso HH è associato a neoplasie umane, compreso il BCC.
Il normale funzionamento della via HH può essere alterato a causa di mutazioni nei geni che codificano per le proteine PTCH1, PTCH2, SMO o SUFU.
PTCH1 Le mutazioni genetiche impediscono alla proteina PTCH1 di legarsi a SMO.
Free SMO consente la crescita cellulare non regolata attivando quanto segue:
- Fattori di trascrizione (proteine che si legano a DNA sequenze e controllo il flusso di informazioni genetiche dal DNA a RNA) GLI1 (associato a glioma oncogene 1; chiamata anche proteina del dito di zinco) e GLI2
- Geni di proliferazione cellulare (ciclina D, ciclina E, myc) e
- Regolatori del processo che prevede la crescita del nuovo vasi sanguigni (angiogenesi).
Principali geni che aumentano il rischio di BCC
Mutazioni in PTCH1, PTCH2, SANTO e SUFU i geni predispongono i pazienti al BCC.
Pazienti con cellula basale nevo sindrome (Sindrome di Gorlin) nascono con un'eredità mutazione uno allele del PTCH1 gene. La mutazione porta a autosomica sindrome dominante Cancro predisposizione. L'allele buono rimanente può essere mutato UV l'esposizione alle radiazioni nel corso della vita, in modo che questi pazienti possano farlo sviluppare Tumori BCC in età più giovane rispetto alla popolazione generale.
- Fino a 70% di persone con BCC sporadico senza sindrome del nevo delle cellule basali abbiamo rattoppato PTCH1 mutazioni genetiche a seguito dell'esposizione alle radiazioni ultraviolette.
- Nel 10-20% di pazienti con BCC sporadico, le mutazioni nel gene SMO consentono la segnalazione non regolamentata di tumore aumentare.
- Un piccolo numero di pazienti con BCC sporadico presenta mutazioni in PTCH1 controparte PTCH2 (una variante di PTCH1) e SUFU.
Altri geni importanti nel rischio di BCC
Mutazioni nel gene soppressore del tumore Q53 e il recettore della melanocortina-1 (MCR1) può essere coinvolto nello sviluppo di BCC sporadico.
Gen P53
- Q53 codifica per la proteina P53 che è stata definita 'guardiana di genoma‘.
- La proteina P53 funziona per rilevare lesioni genotossiche e arrestare la divisione cellulare, consentendo la riparazione del DNA prima della replicazione.
- In caso di danni estesi al DNA, induce apoptosi (morte cellulare) per eliminare i difetti e potenzialmente il malvagio cellule.
- Mutazioni di Q53 si verificano in un'ampia varietà di tumori umani, compreso il BCC.
- In 44-100% di pazienti con BCC, le mutazioni si trovano in Q53, molto probabilmente a causa dell'esposizione ai raggi UV.
- È noto che l'esposizione all'arsenico contribuisce alla formazione di BCC e si ritiene che avvenga attraverso la metilazione del DNA dei geni in Q53 itinerario.
Gene del recettore della melanocortina-1
- il MC1R Codici genetici per la proteina del gene del recettore della melanocortina-1 (MC1R) espressi sulla superficie di melanociti.
- Dopo la stimolazione da α-melanociti-ormone stimolante (αMSH), porta alla produzione di melanina sulla pelle e capelli.
- Se lui MC1R Il gene è di tipo selvatico, eumelanina viene prodotta portando alla pelle abbronzata e ai capelli scuri.
- il MC1R Le varianti di colore dei capelli rossi (RHC) portano alla produzione di feomelanina e RHC fenotipo: pelle chiara, capelli rossi, lentiggini e anziani suscettibilità per melanoma e tumori della pelle non melanoma.
- Diversi studi confermano l'associazione di MC1R varianti con rischio di BCC e mostrano che una carnagione chiara oltre a MC1R Le varianti aumentano notevolmente questo rischio.
Vari geni
Mutazioni / varianti dei seguenti geni possono predisporre i pazienti a BCC sporadico:
- Gene glutatione-S-transferasi (le glutatione-S-transferasi cellulari sono coinvolte nella protezione contro lo stress ossidativo nella pelle)
- P 450 CYP enzima gene (citocromo P450 enzimi sono coinvolti nella disintossicazione di numerosi xenobiotici, tra cui cancerogeno componenti del fumo di tabacco)
- Gene di riparazione del DNA XRCC3
- Cyclindipendente chinasi inibitore geni CDKN2A e CDKN2B
- Basale cheratinociti frenare K5 gene
- BRM gene.
Antagonista del riccio per BCC avanzato
Vismodegib (nome commerciale Erivedge ™) è un inibitore della via del riccio approvato nel 2012 per il trattamento di malattie avanzate e metastatico BCC. Nel 2015 sonidegib è stato approvato anche per il trattamento del carcinoma basocellulare avanzato.
Altre terapie mirate molecole della via di segnalazione HH sono in fase di sviluppo.