Einführung
Im Dezember 2016 genehmigte die US-amerikanische Food and Drug Administration (FDA) Crisaborol aktuell Salbe, 2%, zur Behandlung von leicht bis mittelschwer atopisch Dermatitis bei Patienten ab 2 Jahren. Es ist eine Phosphodiesterase 4 auf Borbasis Inhibitor (PDE-4) und wird als EUCRISA ™ vermarktet. Es wurde von Anacor Pharmaceuticals Inc. (Palo Alto, Kalifornien, USA) entwickelt, die Pfizer Inc (New York, USA) im Mai 2016 erworben hat.
Crisaborol ist eine nichtsteroidale topische Monotherapie, die Phosphodiesterase (PDE) -4 hemmt Enzym auf der Haut. Es wurde gezeigt, dass überaktive PDE-4 zu den Anzeichen und Symptomen einer atopischen Dermatitis beiträgt.
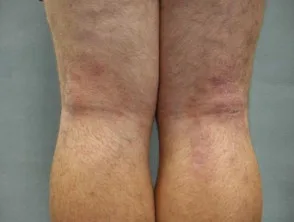
Atopische Dermatitis
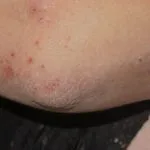
Atopische Dermatitis des Halses
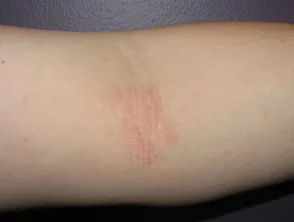
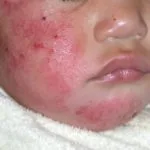
Atopische Dermatitis
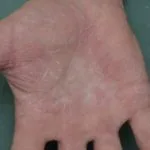
Atopische Dermatitis
Wie funktioniert Chrysaborol?
- Der spezifische Mechanismus oder die spezifischen Mechanismen, durch die Crisaborol seine Wirkung ausübt therapeutisch Die Aktion ist nicht genau definiert.
- Atopische Dermatitis ist durch Typ 2 T (Th2) -Helferzellen gekennzeichnet Entzündung.
- Crisaborol ist ein Inhibitor des PDE-4-Enzyms.
- PDE-4 Hemmung führt zu einer Erhöhung intrazellulär Gehalte an cyclischem Adenosinmonophosphat (cAMP).
- Crisaborol modifiziert die Entzündung bei atopischer Dermatitis, indem es den Abbau von cAMP durch PDE4 hemmt, was zu einer nachfolgenden Modifikation von führt nuklear Faktor-kB und T-Zelle Signalwege.
Dosierung und Anwendung
- Crisaborol ist nur zur topischen Anwendung und nicht zur ophthalmologischen, oralen oder intravaginal verwenden.
- Es wird zweimal täglich als dünne Schicht auf den oder die betroffenen Bereiche aufgetragen.
- Inaktive Inhaltsstoffe in der Salbe umfassen weißes Petrolatum, Propylenglykol, Mono- und Diglyceride, Paraffin, butyliertes Hydroxytoluol und Calciumdinatriumedetat.
Verwendung in bestimmten Populationen
Die Schwangerschaft
- Es liegen keine Daten zur Anwendung von Crisaborol bei schwangeren Frauen vor, um das drogenbedingte Risiko schwerer Geburtsfehler und Fehlgeburten zu ermitteln.
- Nicht nachteilig Entwicklung Effekte wurden bei trächtigen Kaninchen mit oraler Verabreichung von Crisaborol beobachtet.
- Informationen zur Sicherheit von Medikamenten, die während der Schwangerschaft eingenommen werden, finden Sie auf der Seite DermNet NZ.
Stillzeit
- Es gibt keine Informationen über das Vorhandensein von Crisaborol in der Muttermilch oder die Auswirkungen des Arzneimittels auf das stillende Kind nach topischer Anwendung bei stillenden Frauen.
- Crisaborol wird systemisch resorbiert.
- Der potenzielle Nutzen-Risiko-Verhältnis sollte bei der Verschreibung von Crisaborol an die Mutter berücksichtigt werden.
- Weitere Informationen zu Stillen und Haut finden Sie auf der Seite DermNet NZ.
Pädiatrisch verwenden
- Die Sicherheit und Wirksamkeit von Crisaborol bei pädiatrischen Patienten ab 2 Jahren wurde nachgewiesen.
- Die Sicherheit und Wirksamkeit von Crisaborol bei Kindern unter 2 Jahren wurde nicht nachgewiesen.
Geriatrische Anwendung
- Die klinischen Studien mit Crisaborol umfassten nicht genügend Probanden ab 65 Jahren, um festzustellen, ob sie anders ansprechen als jüngere Probanden.
Was sind die möglichen nachteiligen Auswirkungen von Crisaborol?
- Die häufigste Nebenwirkung von Crisaborol sind Schmerzen an der Applikationsstelle wie Brennen oder Stechen.
- Crisaborol kann verursachen Überempfindlichkeit Reaktionen am Applikationsort oder an einem entfernten Ort.
- Diese können schwerwiegend sein und Bienenstöcke umfassen (Kontakt Urtikaria), Juckreiz, Schwellung und Erythem.
- Wenn Anzeichen und Symptome einer Überempfindlichkeit auftreten, sollte Crisaborol sofort abgesetzt und eine geeignete Therapie eingeleitet werden.
- Crisaborole ist kontraindiziert bei Patienten mit bekannter Überempfindlichkeit gegen Crisaborol oder einen Bestandteil der Formulierung.
Crisaborol ist in Phase-3-Studien vielversprechend für atopische Dermatitis
- Crisaborol ist das erste topische nichtsteroidale entzündungshemmende Mittel seiner Art.entzündlich, PDE-Hemmer zur Behandlung von leichter bis mittelschwerer Neurodermitis.
- Crisaborol ist eine vielversprechende nichtsteroidale topische Behandlung zur Verbesserung der Behandlung von Neurodermitis.
- Signifikante Verbesserung der Schwere der Erkrankung, Juckreiz Intensität und alle anderen bewerteten Anzeichen und Symptome einer atopischen Dermatitis deuten darauf hin, dass Crisaborol auf die Pathogenese der Krankheit.
- Die neuartige Borchemie von Chrysaborol ermöglicht Synthese eines Bassesmolekular-gewichtige Verbindung (251 d), die ein effektives Eindringen in die menschliche Haut ermöglicht.
Hilft Crisbarole bei anderen Hauterkrankungen?
Es wurde berichtet, dass Crisaborol in vorteilhaft ist intertriginös/Flexion Psoriasis und Gesichtspsoriasis.