Wat is assistent behandeling?
Adjuvante therapie wordt gedefinieerd als behandeling die wordt toegediend na initiële therapie. In het geval van huid melanomaAdjuvante therapie is een vorm van behandeling die wordt overwogen na een volledige operatie excisie van melanoom (de eerstelijnsbehandeling) [1].
Adjuvante immunotherapie heeft tot doel verspilling te elimineren microscopisch melanoomcellen via het immuunsysteem, om het risico op kanker wederverschijningen om de algehele kans op genezing te verbeteren. [1].
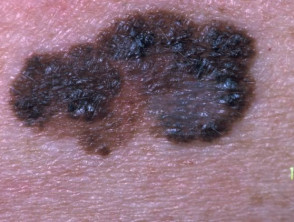
Primair melanoom
Oppervlakkig verspreidend melanoom
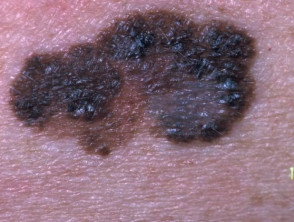
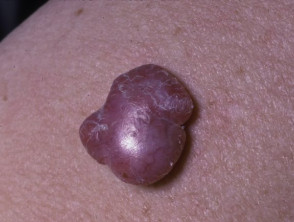
nodulair melanoom
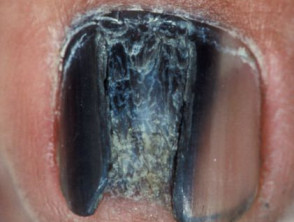
Acraal melanoom
Wie gebruikt adjuvante therapieën?
Indicaties om adjuvante therapieën voor huidmelanoom te overwegen zijn onder meer [1–3]:
- Ongunstig gelegen ziekte – melanoom van gemiddelde dikte (Breslow-dikte > 1 mm) met of zonder extra pathologisch voorspelling factoren zoals ulceratie of verhoogd mitotisch Snelheid
- Fase III metastatisch melanoom (dit is wanneer er sprake is van histologisch bewijs van melanoom in de regio lymfe knooppunt/s, onderweg of via satelliet metastase)
- Gelokaliseerd melanoom met hoog risico op lokaal recidief als gevolg van inadequate excisiemarges of perineural invasie (ook wel neurotropisme).
Wat zijn adjuvante therapieën voor melanoom?
Driver-gerichte immunotherapie en kankertherapie mutaties hebben een voordeel laten zien bij stadium IV gemetastaseerd melanoom (wanneer metastase zijn gedetecteerd). Er is ook gemeld dat adjuvante therapie het relatieve risico op recidief met 40% vermindert bij metastatisch melanoom in stadium III, met een absolute reductie van 15 tot 25% in het risico op lokaal en op afstand recidief. Er zijn nog geen gegevens over de algehele overleving gerapporteerd voor immunotherapie, maar er worden significante voordelen voor de algehele overleving gezien bij dabrafenib en trametinib in combinatie met adjuvans. BRAF-mutant stadium III gemetastaseerd melanoom.
De resultaten van adjuvante behandeling zijn gepubliceerd met behulp van immunotherapie, gerichte therapieof radiotherapie die in totaal maximaal 12 maanden is toegediend.
Immunotherapie
Er zijn twee soorten immuuncellen controle remmers, vanaf 2019.
- de cytotoxisch T-lymfocyt-geassocieerd eiwit 4 (CTLA4) antilichaam, ipilimumab (Yervoy®) [4].
- Geprogrammeerd celdoodeiwit 1 (PD1) antistoffen:
- Nivolumab (Opdiv®) [4]
- Pembrolizumab (Keytruda®) [5].
Immunotherapieën Ze worden elke drie weken toegediend via een intraveneus infuus [4].
Gerichte therapieën
Gerichte therapieën blokkeren de door mitogeen geactiveerde proteïne (MAP) kinase-route [6].
- BRAF-remmers Hiertoe behoren dabrafenib, vemurafenib en encorafenib.
- MEK Remmers zijn onder meer trametinib, cobimetinib en binimetinib.
BRAF-remmers worden tweemaal daags oraal toegediend; A MEK remmer Het wordt over het algemeen eenmaal per dag oraal ingenomen [8]. Een BRAF- en MEK-remmer worden meestal samen in combinatietherapie gebruikt om de tumor resistentie tegen therapie met één middel [7].
Radiotherapie
Stereotactisch Daarna kan uitwendige radiotherapie worden overwogen therapeutisch lymfadenectomie om het tarief te verlagen nodaal herhaling, vooral als er sprake is van een extranodaal uitbreiding van gemetastaseerd melanoom [8,9].
Welke zijn de? contra-indicaties met adjuvante therapieën?
Patiënten met een lager risico of een dun melanoom krijgen doorgaans geen adjuvante behandelingen aangeboden (stadium I/IIA-ziekte) [1,2].
Relatieve contra-indicaties voor het gebruik van immunotherapie zijn onder meer:
- Zwangerschap: vanwege zorgen over mogelijk verlies van de moeder immunologisch tolerantie voor een foetus [10]
- Een geschiedenis van slecht gecontroleerd of ongecontroleerd auto immuun Ziekte: Activering van het immuunsysteem door immuuntherapie kan een verergering van de auto-immuunziekte veroorzaken. [elf]
- Orgaan transplantatie - Er zijn geïsoleerde meldingen geweest van snelle afstoting van het getransplanteerde orgaan bij gebruik van checkpointremmers. Immunotherapie kan nog steeds worden overwogen nier transplantatie patiënten als zij dat ook zijn dialyse kandidaten [12]
- Een ernstige of levensbedreigende tegengestelde reactie op eerdere immunotherapie [13].
Gerichte therapie met BRAF-remmers is dat wel gecontra-indiceerd voor patiënten zonder BRAF V600-controller mutatie [7].
Wat is neoadjuvans behandeling?
In tegenstelling tot adjuvante therapie, die wordt gegeven na een operatie om melanoom te verwijderen, is neoadjuvante therapie een inductie behandeling Het begon vóór de splitsing. Het wordt normaal gesproken gebruikt wanneer de primair melanoom is inoperabel (dat wil zeggen: het is een grote tumor, het excisiedefect kan niet worden gesloten of excisie zou cosmetisch onaanvaardbaar zijn) of wanneer een lymfeklier of diepgeworteld Melanoommetastasen zijn te omvangrijk om veilig te verwijderen. De bedoeling van neoadjuvante therapie is om de tumor te verkleinen zodat een operatie kan worden uitgevoerd. [14].
Wat zijn de voordelen van adjuvante therapie voor stadium III gemetastaseerd melanoom?
De eerste resultaten van klinische onderzoeksprogramma's tonen consistente en klinisch significante voordelen aan van gerichte therapieën en immuuntherapieën bij metastatisch melanoom in stadium III, wanneer het melanoom volledig is verwijderd.
Immunotherapie
De eerste onderzoeksgegevens over ipilimumab-immunotherapie bij gemetastaseerd melanoom in stadium III zijn afkomstig uit twee grote onderzoeken. De 5-jaarskans op algehele overleving verbeterde met 28% en het 5-jaarsrisico op herhaling van gemetastaseerd melanoom verbeterde met 24% in die gevallen gerandomiseerd vergeleken met ipilimumab placebo [15].
- In het CheckMate 238-onderzoek werd de recidiefvrije overleving met 35% verminderd bij degenen die gerandomiseerd waren naar nivolumab vergeleken met ipilimumab, met een vermindering in ernstige gevallen. bijwerkingen [4].
- In het KEYNOTE-054-onderzoek hadden patiënten die gerandomiseerd waren naar pembrolizumab een reductie van 43% in het risico op recidief of overlijden vergeleken met placebo. [5].
Gerichte therapie
Onderzoek naar BRAF en dubbele BRAF/MEK-remmers remming bij patiënten met stadium III gemetastaseerd melanoom werden uitgevoerd vóór immunotherapiestudies. De belangrijkste resultaten vindt u hieronder. Er werd een consistente verbetering in de algehele overleving (OS) van patiënten aangetoond bij gebruik van MEK/BRAF-remming met één middel vergeleken met placebo. Dit voordeel werd vergroot bij dubbele remming [7,16]. Vanwege de bijwerkingen van gerichte therapie kan het nodig zijn dat een van de componenten stopgezet wordt. [17].
| Remmer | CR+PR% | Mediaan PFS, mediane OS |
| Vemurafenib [18] | 53% | 6,9 maanden, 13,6 maanden |
| Dabrafenib [19] | 50% | 6,7 maanden, 18 maanden |
| Trametinib [20] | 22% | 4,8 maanden (alleen PFS) |
| Dabrafenib + trametinib [7] | 67% | 11 maanden, 25,1 maanden |
| Dabrafenib + trametinib versus vemurafenib [16] | 64% | 12,6 maanden, 25,6 maanden |
CR: volledige reactie; PR: gedeeltelijke respons; CR + PR%: percentage patiënten met gedeeltelijke of volledige respons; PFS: progressievrije overleving; OS: algehele overleving
Adjuvante radiotherapie
Lokaal controleren Melanoomkanker kan worden verbeterd met adjuvante radiotherapie als het risico op een lokaal recidief onaanvaardbaar hoog blijft na chirurgische excisie, zoals bij:
- Ongepast brede decolleté marges, vaak als gevolg van anatomische of cosmetische beperkingen rond het oog/bindvlies, neus, lippen of oren [21]
- satelliet verwondingen
- Neurotropisme (perineurale invasie) in histologie [8,9]
- desmoplastisch melanoom, vanwege de neiging tot lokaal recidief.
Hoewel gerandomiseerde gecontroleerde onderzoeken het voordeel van adjuvante radiotherapie niet hebben geëvalueerd, hebben verschillende grote observationele cohorten positieve resultaten gerapporteerd met een verbetering van 50% naar 85% in het risico op lokaal recidief. Mogelijk bewijs van een afname van het recidief van de klier werd ook waargenomen [22-24].
De winkel opruiend De resulterende effecten van radiotherapie kunnen een synergetische impuls geven effectiviteit van immunotherapie [25,26]. Er wordt meer onderzoek gedaan om de voordelen ervan te evalueren. [27,28].
Wat zijn de nadelen van adjuvante therapieën?
De vergelijkende voordelen van immunotherapie met traditionele chemotherapie hebben de spelregels voor de behandeling van gemetastaseerd melanoom bij sommige patiënten veranderd. Bij veel patiënten reageert het melanoom echter niet of slechts gedeeltelijk op immunotherapie. Bovendien zijn gerichte therapieën alleen geïndiceerd voor degenen bij wie het melanoom de BRAF V600-drivermutatie draagt (ongeveer 40 tot 50% van huidmelanomen) [29].
Er zijn nog vragen te beantwoorden over adjuvante therapie bij melanoom.
- Verbetert adjuvante immunotherapie de algehele overleving van patiënten met stadium III gemetastaseerd melanoom?
- Is het beter om adjuvante immunotherapie te geven voor stadium III gemetastaseerd melanoom of te wachten tot stadium IV gemetastaseerd melanoom zich ontwikkelt?
- Als een patiënt een BRAF V600-mutatie heeft, moeten we dan eerst gerichte therapie of immunotherapie gebruiken?
- Zou adjuvante immunotherapie of gerichte therapie het risico op ziekte verminderen als het in een eerder stadium van het melanoom wordt gebruikt? Een onderzoek recruteert momenteel deelnemers om deze vraag te beantwoorden bij stadium IIB-C-melanoom (2019).
Wat zijn de bijwerkingen en risico’s van adjuvante therapieën?
Adjuvante behandelingen worden over het algemeen goed verdragen en hebben een relatief langere korte termijn toxiciteit met gecombineerde BRAF/MEK-remming vergeleken met immunotherapie; er bestaat echter een risico op permanente toxiciteit bij adjuvante immunotherapie.
Bijwerkingen van immunotherapie
Immunotherapie kan bijwerkingen veroorzaken als gevolg van immuunactivatie [13,30]. De hieronder beschreven tarieven gelden voor PD1-remmers (nivolumab en pembrolizumab); Immuungerelateerde bijwerkingen komen vaker voor bij CTLA-4-remming (ipilimumab).
- ~25%-vermoeidheid met een PD1-remmer
- Bond: jeuk, dermatitis, of vitiligo bij ~34%
- Maagdarmkanaal: colitis diarree veroorzaken bij een 13% (het risico is hoger bij de combinatie van ipilimumab en nivolumab)
- Schildklier disfunctie: hyperthyreoïdie of hypothyreoïdie bij ~10%
- Artralgie ~ 7%
- Hepatitis 5-10%
- longontsteking 2-4%
- myositis
- Scherp nier letsel
- Heel soms, hypofysitis.
Zie ook Cutane bijwerkingen van checkpointremmers.
Bijwerkingen van gerichte therapieën
De combinatie van dabrafenib/trametinib veroorzaakt de volgende bijwerkingen [17].
- Pyrexie
- Vermoeidheid
- Misselijkheid
- Hoofdpijn
- Diarree
- braken
- Artralgie
- Dermatitis
- Vooral nieuwe huidkanker geschubd cel carcinoom (a BRAF remmende werking)
- Cardiale effecten (linkerventrikeldisfunctie)
- Oculair effecten (wazig zien, coriorretinopatía)
- long efectos (interstitiële enfermedad pulmonar, neumonitis).
Efectos secundarios de la radioterapia
Los efectos secundarios agudos de la radioterapia pueden incluir [31,32]:
- Pellen
- Erytheem
- Relacionados con los órganos ontsteking Y oedeem (bijv. slokdarmontsteking, mucositis, neumonitis)
- Vermoeidheid.
Los efectos secundarios tardíos de la radioterapia pueden incluir:
- Hypopigmentatie of hyperpigmentatie
- teleangiëctasie
- epidermaal atrofie Y breekbaarheid
- alopecia y sudor klier atrofie
- necrose van zachte stof, cartílago o hueso
- Inducida por radiación maligniteit - plaveiselcellen carcinoma, basaal cel carcinoom.