30. Januar 2020 - Großbritannien und Europa stellen die Vermarktung von Picato® ein Gel.
Die Regulierungsbehörde für Arzneimittel und Gesundheitsprodukte, Vereinigtes Königreich [1] und die Europäische Arzneimittel-Agentur (EMA) [2] haben bekannt gegeben, dass die Vermarktung des Picato®-Gels, das Ingenolmebutat enthält, eingestellt wurde. Sie haben empfohlen, dass Patienten die Verwendung des Produkts einstellen, bis eine Untersuchung seiner Sicherheit in Bezug auf die Haut durchgeführt wurde. Krebs.
Mehr sehen:
- Die europäische Vermarktung von Picato wird ausgesetzt, während das Hautkrebsrisiko überprüft wird. 17. Januar 2020. Medscape Medical News.
- Klasse 2 Drogen Merken: LEO Laboratories Ltd, Picato 150 µg / g Gel. 27. Januar 2020. Gouverneur des Vereinigten Königreichs
Einführung
Die FDA-Zulassung für die Verwendung von Ingenolmebutat-Gel basierte auf Daten aus vier Phase-III-Studien mit mehr als 1.000 Personen, die zeigten, dass Ingenolmebutat-Gel, einmal täglich an zwei bis drei aufeinanderfolgenden Tagen aufgetragen, signifikant wirksamer ist als Placebo beim ausräumen aktinisch Keratose.
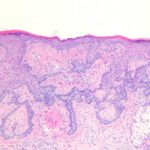
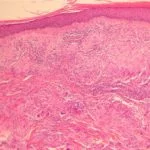
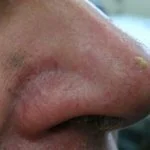
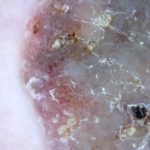
Aktinisch Keratose von Gesicht und Kopfhaut
In zwei Doppelblind, Fahrzeug-in kontrollierten klinischen Studien wurden 547 erwachsene Probanden mit aktinischer Keratose im Gesicht oder auf der Kopfhaut behandelt zufällig bis zur Behandlung mit 0,015% Ingenolmebutat-Gel oder Vehikel-Gel an 3 aufeinanderfolgenden Tagen, gefolgt von einer 8-wöchigen Nachbeobachtungszeit.
Die Studien umfassten Probanden mit 4 bis 8 klinisch typischen, sichtbaren, diskret Aktinische Keratosen innerhalb von 25 cm2 Angrenzender Behandlungsraum.
An jedem planmäßigen Dosierungstag wurde das Studiengel auf den gesamten Behandlungsbereich aufgetragen. Insgesamt 536 Probanden (98%) schlossen diese Studien ab. Die Studienteilnehmer waren zwischen 34 und 89 Jahre alt (halb 64 Jahre). Ungefähr 85% der Probanden waren männlich und alle mit Ingenolmebutat behandelten Probanden waren Kaukasier.
Wirksamkeit sie wurde an Tag 57 beurteilt. Die vollständige Clearance-Rate wurde als der Anteil der Probanden ohne klinisch sichtbare AKs im Behandlungsbereich definiert.
Die partielle Clearance-Rate wurde als der Anteil der Probanden mit einer Verringerung der Anzahl aktinischer Keratosen um 75% oder mehr definiert. Verletzungen zu Base im gewählten Behandlungsgebiet.
Die wichtigsten Ergebnisse sind unten tabellarisch aufgeführt.
| Studie 1 | Studie 2 | |||
|---|---|---|---|---|
| Ingenolmebutat-Gel, 0,015% (n=135) | Fahrzeug (n = 134) | Ingenolmebutat-Gel, 0,015% (n=142) | Fahrzeug (n = 136) | |
| Vollständige vollständige Eliminierung an Tag 57 | 50 (37%) | 3 (2%) | 67 (47%) | 7 (5%) |
| Teilweise totale Elimination an Tag 57 | 81 (60%) | 9 (7%) | 96 (68%) | 11 (8%) |
| Vollständige Entfernung von Kopfhautläsionen (Tag 57) | 4/26 (15%) | 0/25 (0%) | 31/9 (29%) | 1/25 (4%) |
| Vollständige Entfernung von Gesichtsläsionen (Tag 57) | 46/109 (42%) | 3/109 (2%) | 58/111 (52%) | 6/111 (5%) |
- Patienten, die bis Tag 57 in Studie 1 und Studie 2 eine vollständige Clearance erreicht hatten, traten in eine 12-monatige Nachbeobachtungsphase ein.
- Basierend auf 108 mit Ingenolmebutat-Gel behandelten Patienten, die in Studie 1 und Studie 2 eine vollständige Clearance erreichten Wiedererscheinen die Rate nach 12 Monaten betrug 54%.
- Rezidiv wurde definiert als der Prozentsatz der Probanden mit AKs, die in dem zuvor behandelten Bereich identifiziert wurden und die bis Tag 57 eine vollständige Abheilung erreichten.
Aktinische Keratose des Rumpfes und der Extremitäten
In zwei Vehikel-kontrollierten, doppelblinden klinischen Studien wurden 458 erwachsene Probanden mit aktinischer Keratose am Rumpf oder an den Extremitäten randomisiert einer Behandlung mit Ingenolmebutat 0,051 TP1T-Gel oder Vehikel-Gel für 2 aufeinanderfolgende Tage, gefolgt von 8 aufeinanderfolgenden Nachbeobachtungstagen, zugeteilt .Wochen. -Zeitraum. Die Studien umfassten Probanden mit 4 bis 8 klinisch typischen, sichtbaren, diskreten aktinischen Keratoseläsionen innerhalb eines Radius von 25 cm.2 Angrenzender Behandlungsraum. Hypertrophe und hyperkeratotisch Läsionen wurden von der Behandlung ausgeschlossen. An jedem planmäßigen Dosierungstag wurde das Studiengel auf den gesamten Behandlungsbereich aufgetragen. Insgesamt 447 Probanden (98%) schlossen diese Studien ab. Die Studienteilnehmer waren zwischen 34 und 89 Jahre alt (Durchschnitt 66 Jahre).
Ungefähr 62% der Probanden waren männlich und alle mit Ingenolmebutat behandelten Probanden waren Kaukasier.
Vollständige und teilweise Clearance-Raten wurden wie in Studie 1 definiert.
Die wichtigsten Ergebnisse sind unten tabellarisch aufgeführt.
| Atelier 3 | Atelier 4 | |||
|---|---|---|---|---|
| Ingenolmebutat-Gel, 0,05% (n=126) | Fahrzeug (n = 129) | Ingenolmebutat-Gel, 0,05% (n=100) | Fahrzeug (n = 103) | |
| Vollständige vollständige Eliminierung an Tag 57 | 35 (28%) | fünfundsechzig%) | 42 (42%) | 5 (5%) |
| Globale Teilclearance an Tag 57 (≥75%) | 56 (44%) | 9 (7%) | 55 (55%) | 7 (7%) |
| Armläsionen mit vollständiger Heilung (CR) (Tag 57) | 22/84 (26%) | 4/82 (5%) | 27/59 (46%) | 3/67 (5%) |
| CR Handverletzungen (Tag 57) | 4/25 (16%) | 0/29 (0%) | 6/28 (21%) | 0/27 (0%) |
| CR-Brustläsionen (Tag 57) | 8/9 (89%) | 1/8 (13%) | 3/5 (60%) | 1/3 (33%) |
| CR (Bein/Schulter/Rücken) | 1/8 (13%) | 1/10 (10%) | 6/8 (75%) | 1/6 (17%) |
- Patienten, die an Tag 57 in Studie 4 eine vollständige Heilung erreichten, traten in eine 12-monatige Nachbeobachtungsphase ein. Basierend auf 38 mit Ingenolmebutat-Gel behandelten Patienten, die in Studie 4 eine vollständige Clearance erreichten, betrug die 12-Monats-Rezidivrate 50%.
- Das Wiederauftreten wurde als Prozentsatz der Patienten mit identifizierter aktinischer Keratose definiert Verletzung im zuvor behandelten Bereich, der am Tag 57 vollständig beseitigt wurde.
Zur Bewertung wurden keine Langzeitstudien an Tieren durchgeführt krebserregend Potenzial von Ingenolmebutat.
Die Auswirkungen von Ingenolmebutat auf die Fertilität wurden nicht untersucht.
Anwendung bei älteren Menschen
- Von 1165 Probanden, die in klinischen Studien mit Ingenolmebutat-Gel behandelt wurden, war 56% 65 Jahre oder älter und 21% 75 Jahre oder älter.
- Insgesamt wurden keine Unterschiede in der Sicherheit oder Wirksamkeit zwischen diesen Probanden und jüngeren Probanden beobachtet.
Mehr Informationen
Zurück zur Ingenolmebutat-Gel-Seite.