Orales Alitretinoin für die Hand Ekzem
Toctino® (orales Alitretinoin) wird von Stiefel Laboratories (UK) vertrieben und ist für die Behandlung von Handekzemen in Großbritannien, Europa, Israel und Kanada (Februar 2013) zugelassen.
Sicherheit und Wirksamkeit orales Alitretinoin bei Patienten mit schwerer chronisch Handekzem feuerfest zu aktuell Kortikosteroide wurde in zwei etabliert zufällig, doppelblind, Placebo-Kontrollierte Phase-3-Studien.
Studie 1
Der BACH (Nutzen von Alitretinoin in chronischen Händen Dermatitis Studie) umfasste 1.032 Patienten mit schwerem chronischem Handekzem / Dermatitis, die nicht ansprachen oder vorübergehend Ansprechen (anfängliche Besserung und Verschlechterung der Krankheit trotz fortgesetzter Behandlung) auf starke topische Kortikosteroide oder auf Intoleranz gegenüber starken topischen Kortikosteroiden.
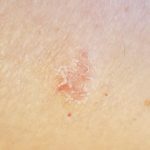
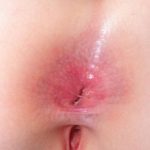
Alle Phänotypen von Handekzemen enthalten: Hyperkeratose (87%), Pompholyx (27%), Fingerspitzendermatitis (43%) und andere (15%). Grundsätzlich hatten alle Patienten Hautzeichen. Entzündung, bestehend aus Erythem mich Vesikel.
das primär Der Endpunkt in diesen Studien war der Anteil der Patienten, die am Ende der Therapie PGA-Werte (Physicians Global Assessment) für saubere oder nahezu saubere Hände erreichten. Die Behandlungsdauer betrug 12 bis 24 Wochen.
Die Behandlung mit Alitretinoin führte zu einem signifikant höheren Anteil von Patienten, die im Vergleich zu Placebo saubere / nahezu saubere Hände erreichten. Die Antwort war Dosis-abhängig. Die Ansprechraten für die verschiedenen EHC-Subtypen waren mit Ausnahme von Pompholyx-Patienten ebenfalls dosisabhängig.
| Alitretinoin | |||
|---|---|---|---|
| Hauptvariable | 10 mg | 30 mg | Placebo |
| Intent-to-Treat (ITT) -Population | N = 418 | N = 409 | N = 205 |
| Physician Global Assessment (PGA): | |||
| Gesamtantwortrate | 115 (27,5%) | 195 (47,7%) | 34 (16,6%) |
| klar | 39 (9,3%) | 90 (22,0%) | 6 (2,9%) |
| Fast klar | 76 (18,2%) | 105 (25,7%) | 28 (13,7%) |
| Vergleich mit Placebo | P = 0,004 | P = <0,001 | n / a |
| CHE-Subtyp | Hyperkeratose | Hyperkeratose / Pompholyx | Pompholyx |
|---|---|---|---|
| % Bevölkerung ITT | 64% | 22% | 5% |
| Rücklaufquote (PGA) | 30 mg: 54% | 30 mg: 33% | 30 mg: 33% |
| 10 mg: 30% | 10 mg: 23% | 10 mg: 22% | |
| Placebo: 12% | Placebo: 12% | Placebo: 30% |
Patienten mit sauberen / fast sauberen Händen am Ende der Behandlung wurden weitere 24 Wochen beobachtet. Während dieser Zeit war keine aktive medikamentöse Behandlung für CHE zulässig. Rückfall wurde als 75% der anfänglichen Summe definiert Verletzung Symptom Interpunktion.
In dieser Analyse trat die Mehrheit der Responder, die 10 mg und 30 mg Alitretinoin erhielten, am Ende der Nachbeobachtungszeit nicht zurück.
Rückfallraten * am Ende der Nachuntersuchung
| Alitretinoin | Placebo | ||
|---|---|---|---|
| 10 mg | 30 mg | ||
| N = 418 | N = 409 | N = 205 | |
| Antwortende | 115 (100%) | 195 (100%) | 34 (100%) |
| Kein Rückfall | 81 (70,4%) | 122 (62,6%) | 19 (55,9%) |
* Entspricht einer Berechnung der zuletzt bewegten Beobachtung (LOCF)
Studie 2
Eine Folgestudie (die zweite Phase-3-Studie) untersuchte die Wirksamkeit und Sicherheit eines zweiten Behandlungszyklus sowohl bei Patienten, die zuvor auf die Behandlung ansprachen und dann einen Rückfall erlitten (Kohorte A), als auch bei Patienten, die nicht auf die Behandlung ansprachen (Kohorte B). . Patienten der Kohorte A wurden randomisiert auf die gleiche Alitretinoin-Dosis wie bei der Erstbehandlung oder auf Placebo im Verhältnis 2: 1 eingestellt.
Die 80% von rezidivierten Patienten in Kohorte A, die eine wiederholte Behandlung mit 30 mg Alitretinoin erhielten, erzielten saubere / fast saubere Hände im Vergleich zu 8% in der Placebogruppe (p <0,001).
Die 48% der rezidivierten Patienten in Kohorte A, die mit 10 mg Alitretinoin behandelt wurden, erreichten saubere / fast saubere Hände im Vergleich zu 10% in der Placebogruppe (p = 0,1).
Alitretinoin Gel 0,1% für Kaposi Sarkom
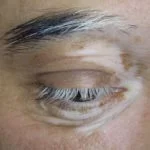
Alitretinoin-Gel (Panretin®; Ligand Pharmaceuticals USA) wurde von der US-amerikanischen FDA zur Behandlung von zugelassen Haut- Verletzungen im Kaposi-Sarkom (KS) im Jahr 1999. Seitdem ist das Medikament in Europa und Kanada zugelassen.
Zwei multizentrische, prospektive, randomisierte, Doppelblind, FahrzeugIn kontrollierten Studien wurde die Wirksamkeit von Alitretinoin-Gel bei Patienten mit AIDS-bedingten KS-Hautläsionen bewertet.
In beiden Studien war der primäre Endpunkt der Wirksamkeit die Haut-KS. Tumor Ansprechrate nach 12-wöchiger Behandlung mit dem Studienmedikament.
Die KS-Tumorantwortrate wurde bewertet, indem 3 bis 8 KS-Indexläsionen gemäß den modifizierten Antwortkriterien der AIDS Clinical Trials Group (ACTG) bewertet wurden, die auf die topische Therapie angewendet wurden (d. H. Bewertung der Körpergröße und nur Bereich der Indexläsionen; progressiv Die Krankheit wurde nur bei behandelten Indexläsionen und nicht bei Nicht-Indexläsionen und neuen Läsionen bewertet.
Die FDA überprüfte Fotos von Läsionen bei Patienten, die nach den modifizierten ACTG-Kriterien als Responder angesehen wurden, auf eine kosmetisch vorteilhafte Reaktion, definiert als eine Verbesserung des Erscheinungsbilds um mindestens 50% im Vergleich zu Basein mindestens 50% der Indexläsionen und mindestens 3 Wochen lang aufrechterhalten.
Eine globale Bewertung durch Ärzte wurde ebenfalls durchgeführt. Es wurden alle behandelten Läsionen des Patienten (Index und andere) im Vergleich zum Ausgangswert berücksichtigt. In dieser Bewertung wurden Patienten mit einer Verbesserung der KS-Läsionen um mindestens 50% als Responder angesehen.
Studie 1
Insgesamt 268 Patienten wurden aus Zentren in den USA und Kanada aufgenommen.
Die Patienten wurden behandelt aktuell drei- bis viermal täglich mit Alitretinoin-Gel oder einem entsprechenden Trägergel für mindestens 12 Wochen.
Reaktionen auf Alitretinoin-Gel wurden sowohl bei zuvor unbehandelten Patienten als auch bei Patienten mit beobachtet systemisch und / oder topische Behandlung für KS.
| Parameter | Alitretinoin-Gel (n = 134) | Vehikelgel (n = 134) |
|---|---|---|
| Modifizierte ACTG-Reaktion (Indexläsionen) | 34% (Teilantwort) 1% (vollständige Antwort) |
16% (Teilantwort) p = 0,0012 |
| Gesamtbewertung des Arztes (alle behandelten Verletzungen) | 19% (Teilantwort) | 4% (Teilantwort) P = 0,00014 |
| Nützliche Antwortfotos (nur Indexläsionen) | 15% | 4% p = 0,0026 |
Studie 2
Studie 2 war eine internationale Studie mit einer geplanten Aufnahme von 270 Patienten.
Die Studie wurde aufgrund vorläufiger positiver Ergebnisse im ursprünglichen Datensatz von 82 Patienten vorzeitig abgebrochen.
Die Patienten wurden 12 Wochen lang zweimal täglich topisch mit Alitretinoin-Gel oder einem entsprechenden Vehikel behandelt.
Reaktionen auf Alitretinoin-Gel wurden sowohl bei zuvor unbehandelten Patienten als auch bei Patienten mit vorheriger Behandlung von systemischer und / oder topischer KS beobachtet.
| Parameter | Alitretinoin-Gel (n = 36) | Vehikelgel (n = 46) |
|---|---|---|
| Modifizierte ACTG-Reaktion (Indexläsionen) | 36% (Teilantwort) | 7% (Teilantwort) |
| Gesamtbewertung des Arztes (alle behandelten Verletzungen) | 47% (Teilantwort) | 11% (Teilantwort) |
| Nützliche Antwortfotos (nur Indexläsionen) | 19% | 2% |
In beiden Studien traten Reaktionen bei Patienten mit einem breiten CD4 + -Basisbereich auf. Lymphozyten Zählungen, einschließlich Patienten mit CD4 + -Lymphozytenzahlen von weniger als 50 Zellen / mm3. Fast alle Patienten erhielten begleitend antiretrovirale Kombinationstherapie.