Anzeige
Hautkrebs
Anwendung zur Erleichterung der Selbstuntersuchung und Früherkennung der Haut. Weiterlesen.
Was ist Pembrolizumab?
Pembrolizumab (früher bekannt als Lambrolizumab; Handelsname Keytruda®) ist ein von Merck and Co (New Jersey, USA) vermarktetes Medikament, das auf den programmierten Zelltod 1 (PD-1) abzielt. Empfänger. Das Arzneimittel ist zur Anwendung in der Behandlung bestimmt metastatisch Melanom.
Am 4. September 2014 hat die US-amerikanische Food and Drug Administration (FDA) Pembrolizumab als bahnbrechende Therapie zur Behandlung des metastasierten Melanoms zugelassen. Es wurde im September 2015 in Neuseeland zur Behandlung von fortgeschrittenem Melanom zugelassen und von der New Zealand Pharmaceutical Management Agency (PHARMAC) für einige Patienten mit finanziert nicht resezierbar oder metastasierendem Melanom ab September 2016. Pembrolizumab wird auch bei metastasiertem nicht-kleinzelligem Lungengewebe angewendet Karzinom, einige Fälle von Hodgkin Lymphom, Urothelkarzinom (März 2018) und Haut- schuppig Zellkarzinom (FDA, Juni 2020). Pembrolizumab wird bei anderen bösartigen Erkrankungen untersucht. Es wurde berichtet, dass es bei Patienten mit Metastasen eine gewisse Wirkung hat. Merkels Zelle Karzinom.
Metastasiertes Melanom
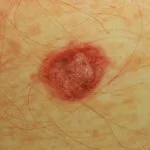
Metastasierung des Hautmelanoms
Kutane Melanommetastasen
Kutane Melanommetastasen
Welche Melanompatienten profitieren von einer Behandlung mit Pembrolizumab?
Pembrolizumab ist angezeigt für die Behandlung von Patienten mit inoperablem oder metastasiertem Melanom.
Siehe wichtige Evidenz aus klinischen Studien zu Pembrolizumab.
Kombinationstherapie mit anderen immunologisch Drogen und gezielt Krebs Die Therapie wird derzeit untersucht und kann die Ansprechraten verbessern.
Wie wirkt Pembrolizumab?
Der programmierte Todesrezeptor (PD-1) ist eine Oberfläche Molekül Ausgedrückt Antigen-stimuliert T-Zellen so viel wie Monozyten, B-Zellenund dendritische Zellen. In normalen Zellen fungiert der PD-1-Rezeptor als Immun-Checkpoint-Rezeptor, der eine Selbsttoleranz von T-Zellen verhindert Autoimmun Reaktionen.
Wenn es nicht gebunden ist, ermöglicht PD-1 eine normale Reaktion auf T-Zellen fortfahren. Die Bindung von PD-1 an seine Liganden, den programmierten Todesrezeptor-Liganden 1 (PD-L1) und den programmierten Zelltod-Liganden 2 (PD-L2), unterdrückt jedoch die Immunantwort, indem eine nachgeschaltete Signalübertragung induziert wird, die die Proliferation von T-Zellen, Zytokin Freisetzung und Zytotoxizität.
Eine abnormale Expression von PD-L1 auf der Oberfläche von Melanomzellen aktiviert PD-1 und unterdrückt es zytotoxisch T-Zelle die Übung. Diese Toleranz von T-Zellen ermöglicht Tumor Zellen, um der Erkennung und dem Angriff durch das Immunsystem zu entgehen.
Pembrolizumab ist ein hochselektives humanisiertes. monoklonal Immunoglobulin G4 (IgG4) Antikörper das an den PD-1-Rezeptor bindet und seine Wechselwirkung mit PD-L1 und PD-L2 blockiert, wodurch der PD-1-vermittelte Weg freigesetzt wird Hemmung der Immunantwort gegen Tumorzellen.
Wie wird Pembrolizumab verabreicht?
- Die empfohlene Pembrolizumab-Dosis beträgt 2 mg/kg, verabreicht als intravenöse Infusion über 30 Minuten alle 3 Wochen, bis die Erkrankung fortschreitet oder nicht mehr akzeptabel ist. Toxizität.
- Pembrolizumab sollte bei folgenden Patienten abgesetzt werden Nebenwirkungen: Note 2 Pneumonitis, Klasse 2 oder 3 Kolitis, Note 2 Nephritis, 3. Klasse Hyperthyreose, Aspartat-Aminotransferase (AST) oder Alanin-Aminotransferase (ALT) > 3 und bis zum 5-fachen der Obergrenze des Normalwerts (ULN) oder insgesamt Bilirubin > 1,5 und bis zum 3-fachen der ULN. Zusätzlich zum Absetzen dieses Medikaments wird ein Zyklus der Verjüngung durchgeführt Kortikosteroide gestartet werden kann.
- Pembrolizumab könnte bei Patienten wieder aufgenommen werden, deren Nebenwirkungen sich auf Grad 0 oder 1 zurückbilden.
- Das Medikament sollte bei Grad 3 oder 4 Nebenwirkungen und wann dauerhaft abgesetzt werden Kortikosteroid Die Dosis für Nebenwirkungen darf in 12 Wochen nicht unter 10 mg/kg/Tag reduziert werden.
Mögliche Arzneimittelwechselwirkungen mit Pembrolizumab
Nicht formell Pharmakokinetik Mit Pembrolizumab wurden Wechselwirkungsstudien durchgeführt.
Welche Nebenwirkungen kann Pembrolizumab verursachen?
In klinischen Studien waren die häufigsten Nebenwirkungen (≥ 20%) bei Patienten, die Pembrolizumab 2 mg/kg alle 3 Wochen erhielten:
- Ermüden
- Husten
- Übelkeit
- Pruritus (hacken)
- Eruption (Nicht spezifiziert)
- Verminderter Appetit
- Verstopfung
- Arthralgie
- Durchfall.
Die häufigste (≥ 2%) schwere Arzneimittelnebenwirkungen mit Pembrolizumab beobachtet wurden Nieren- Insuffizienz, Dyspnoe (Kurzatmigkeit), Lungenentzündung und Zellulitis. Pembrolizumab kann auch Infusionsreaktionen hervorrufen, einschließlich Anaphylaxie.
Pembrolizumab hat auch das Potenzial, schwerwiegende immunvermittelte Nebenwirkungen zu verursachen. Bei 411 Teilnehmern einer klinischen Studie mit fortgeschrittenem Melanom, die mit Pembrolizumab behandelt wurden, waren schwerwiegende immunvermittelte unerwünschte Ereignisse Pneumonitis, Colitis, Hypophysitis (Entzündung von Hypophyse Drüse), Hyperthyreose, Hypothyreose und ein anderer Endokrinopathien, Nephritis u Hepatitis. Später wurde über andere Autoimmunerkrankungen im Zusammenhang mit Pembrolizumab berichtet.
Hautnebenwirkungen
In einem Bericht wurden kutane Nebenwirkungen beschrieben, die bei 35 von 83 (42%) mit Pembrolizumab behandelten Patienten auftraten. das Entwicklung von Hautproblemen war mit längeren Intervallen ohne Progression verbunden. Fallberichte haben andere Hautprobleme während der Zeit nach der Markteinführung des Medikaments beschrieben; Zu diesen Hautproblemen gehörten:
- Morbilliform Eruption
- Pruritus
- Flechte Eruption
- Schuppenflechte
- Ekzem
- Vitiligo und Poliose (Aufhellung von Haar)
- Stomatitis
- Bullös Pemphigoid
- Sarkoid-Ich mag das Granulom
- Panniculitis
- Stevens - Johnson Syndrom / giftig epidermal Nekrolyse
- Multiple Keratoakanthome.
Bei einigen Patienten, die PD-1 einnahmen, wurde über eine Verdunkelung der Haare berichtet Inhibitoren für nicht-kleinzelligen Lungenkrebs.
Siehe auch Hautnebenwirkungen von Checkpoint-Inhibitoren.
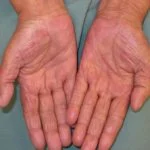
Pembrolizumab-induzierte Psoriasis
Pembrolizumab-induzierte Psoriasis
Pembrolizumab-induzierte Psoriasis
Pembrolizumab-induzierte Psoriasis
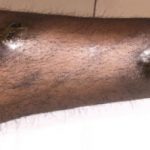
Pembrolizumab-induziertes Ekzem
Pembrolizumab-induziertes Ekzem
Pembrolizumab-induziertes Ekzem
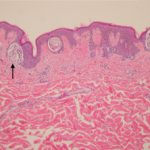
Pembrolizumab-induziertes bullöses Pemphigoid
Pembrolizumab-induziertes bullöses Pemphigoid
Pembrolizumab-induziertes bullöses Pemphigoid
Pembrolizumab-induziertes bullöses Pemphigoid
Die Anwendung von Pembrolizumab in bestimmten Populationen
Schwangere Frau
- Pembrolizumab kann den Fötus schädigen, wenn es einer schwangeren Frau verabreicht wird. Es ist während der Schwangerschaft als Medikament der FDA-Kategorie D aufgeführt.
- In tierexperimentellen Studien gehörten zu den potenziellen Risiken der Verabreichung von Pembrolizumab während der Schwangerschaft erhöhte Raten von Fehlgeburten oder Totgeburten.
- Es ist bekannt, dass menschliches IgG, einschließlich IgG4, die Plazenta passiert; Daher kann Pembrolizumab möglicherweise von der Mutter auf das Kind übertragen werden. Entwicklung Fötus.
- Je nach Wirkmechanismus kann die Exposition des Fötus gegenüber Pembrolizumab das Risiko erhöhen, immunvermittelte Erkrankungen zu entwickeln oder die normale Immunantwort zu verändern.
Stillende Mutter
Es ist nicht bekannt, ob Pembrolizumab oder seine Metaboliten werden in die Muttermilch ausgeschieden. Da viele Medikamente in die Muttermilch ausgeschieden werden, sollten Mütter vor der Anwendung von Pembrolizumab aufhören zu stillen.
Kinder
Die Sicherheit und Wirksamkeit von Pembrolizumab bei Kindern ist nicht erwiesen.
Alte Leute
In einer Studie mit 411 mit Pembrolizumab behandelten klinischen Studienpatienten waren 39% 65 Jahre oder älter. Es gibt keine generellen Unterschiede in Sicherheit bzw Wirksamkeit wurden bei älteren und jüngeren Patienten berichtet.
Patienten mit Nierenversagen
Basierend auf einer populationspharmakokinetischen Analyse ist bei Patienten mit Niereninsuffizienz keine Dosisanpassung erforderlich.
Patienten mit hepatisch Behinderung
Basierend auf einer populationspharmakokinetischen Analyse ist bei Patienten mit leichter Leberfunktionsstörung keine Dosisanpassung erforderlich. Pembrolizumab wurde bei Patienten mit mittelschwerer oder schwerer Leberfunktionsstörung nicht untersucht.