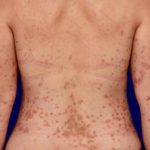
introduzione
Il 26 agosto 2013, la Food and Drug Administration (FDA) statunitense ha approvato la brimonidina (Mirvaso®) attuale gel, 0.33% * (Galderma Laboratories, Texas, USA) Per il trattamento topico di persistente (no-transitorio) facciale eritema (arrossamento) della rosacea negli adulti di età pari o superiore a 18 anni.
È il primo e unico trattamento topico approvato dalla FDA sviluppato e indicato specificamente per l'eritema facciale persistente nella rosacea.
Prove da studi clinici per la brimonidina
L'approvazione del gel topico alla brimonidina si è basata sui dati raccolti da più di 550 pazienti arruolati in due studi clinici di fase 3, ciascuno della durata di un mese. I risultati di entrambi gli studi hanno mostrato che gli adulti che usano Mirvaso hanno dimostrato un miglioramento significativamente maggiore dell'arrossamento del viso da rosacea rispetto a veicolo gel. Inoltre, è stato condotto anche uno studio a lungo termine su 276 soggetti che hanno utilizzato gel di brimonidina topica per un massimo di 12 mesi.
Studi a breve termine 1 e 2
- Entrambi gli studi sono stati randomizzati, doppio cieco, studi clinici controllati dal veicolo.
- Gli studi hanno incluso 553 soggetti di età pari o superiore a 18 anni con eritema facciale rosacea persistente moderato o grave.
- I pazienti sono stati trattati una volta al giorno per 4 settimane con veicolo o gel per uso topico Mirvaso.
- Complessivamente, 99% dei soggetti erano caucasici e 76% erano donne.
- Base la gravità della malattia è stata classificata da una valutazione clinica dell'eritema a 5 punti (CEA) scala e una scala di autovalutazione del paziente a 5 punti (PSA), in cui i soggetti hanno ottenuto punteggi "moderati" o "gravi" in entrambi bilancia.
- il primario efficacia L'endpoint in entrambi gli studi registrativi era il successo composito di 2 gradi, definito come la percentuale di soggetti con un miglioramento di 2 gradi sia in CEA che in PSA misurata a 3, 6, 9 e 12 ore il giorno 29.
- Oltre al giorno 29, l'efficacia è stata valutata il giorno 15 e il giorno 1.
I principali risultati di efficacia sono riassunti nella tabella e nelle figure seguenti.
| Successo* | Studio 1 | Studio 2 | ||
|---|---|---|---|---|
| Gel topico Mirvaso® (N = 129) | Gel per veicoli (N = 131) | Gel topico Mirvaso® (N = 148) | Gel per veicoli (N = 145) | |
| Ora 3 | 31% | 11% | 25% | 9% |
| Ora 6 | 30% | 10% | 25% | 9% |
| Ora 9 | 26% | 10% | 18% | 11% |
| Ora 12 | 23% | 9% | 22% | 10% |
* Miglioramento di 2 gradi nel CEA e miglioramento di 2 gradi sulla scala PSA al giorno 29
Reazioni avverse negli studi 1 e 2
Le reazioni avverse riportate in 330 persone trattate con gel di brimonidina topica applicato una volta al giorno per 29 giorni sono riassunte nella tabella sottostante.
| Gel topico Mirvaso® (N = 330) N. pazienti (%) | Veicolo gel (N = 331) N. pazienti (%) | |
|---|---|---|
| Eritema | 12 (4%) | 3 (1%) |
| Arrossamento | 9 (3%) | 0 |
| Sensazione di bruciore sulla pelle | 5 (2%) | 2 (1%) |
| Dermatite | 3 (1%) | 1 (<1%) |
| Parestesia (formicolio / pungente) | 2 (1%) | 1 (<1%) |
| Acne | 2 (1%) | 1 (<1%) |
| Vista annebbiata | 2 (1%) | 0 |
| Congestione nasale | 2 (1%) | 0 |
Aperto studio a lungo termine
- Uno studio in aperto sul gel di brimonidina topica applicato una volta al giorno per un massimo di un anno è stato condotto in persone con eritema facciale rosacea persistente (non transitorio).
- I pazienti sono stati autorizzati a utilizzare altre terapie per la rosacea.
- Un totale di 276 soggetti ha applicato gel di brimonidina topica per almeno un anno.
- Il più comune eventi avversi riportati sono stati vampate di calore (10%), eritema (8%), aumento della rosacea (5%), rinofaringite (5%), sensazione di bruciore sulla pelle (4%), aumento della pressione intraoculare (4%) e mal di testa (4%).