Wat is guselkumab?
Guselkumab is een biologische behandeling die geïndiceerd is voor matige tot ernstige psoriasis.
De Amerikaanse Food and Drug Administration (FDA) heeft guselkumab (Tremfya™, Janssen Biotech, PA, VS) goedgekeurd voor de behandeling van volwassenen met een matige tot ernstige ziekte. nummerplaat psoriasis die in aanmerking komen voor systemisch therapie of fototherapie. Guselkumab is de eerste en enige goedgekeurde biologische therapie die alleen selectief blokkeert interleukine 23 (IL-23), op cytokine die een sleutelrol speelt bij plaque psoriasis.
Aanvragen voor goedkeuring van guselkumab in de Europese Unie, Japan en andere landen worden momenteel beoordeeld.
In juli 2020 keurde de FDA guselkumab goed voor de behandeling van psoriasis. artritis.
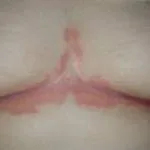
ernstige plaquepsoriasis
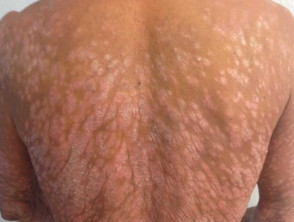
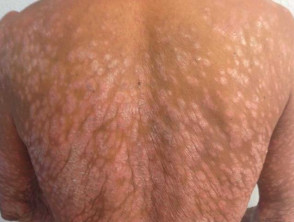
Ernstige psoriasis die de rug aantast
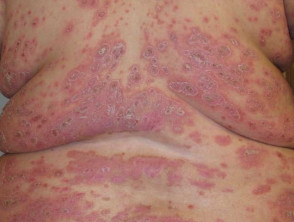
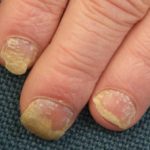
ernstige psoriasis
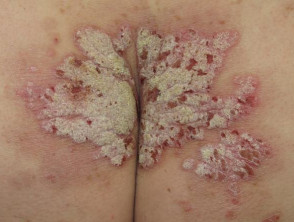
ernstige psoriasis billen
Waar wordt guselkumab voor gebruikt?
- Guselkumab wordt gebruikt voor de behandeling van volwassen patiënten met matige tot ernstige plaque psoriasis die in aanmerking komen voor systemische therapie of fototherapie (ultraviolette straling behandeling).
- Het is niet bekend of guselkumab veilig en effectief is bij kinderen onder de 18 jaar.
Hoe werkt guselkumab?
- Guselkumab is een mens monoklonaal immunoglobuline G1 lambda (IgG1λ) antilichaam dat selectief bindt aan de p19-subeenheid van IL-23 (a eiwit Betrokken in de opruiend respons) en remt de interactie met IL-23 ontvanger.
- Hoewel IL-23 normale ontstekings- en immuunresponsen bevordert, blijken de p19- en p40-subeenheden van IL-23 tot overexpressie te komen bij psoriasis en andere aandoeningen. auto immuun inflammatoire huidziekten.
- Guselkumab bindt zich selectief aan de p19-subeenheid van IL-23 in dendritische cellen Y keratinocyten en blokkeert de interactie met de IL-23-receptor, die ook de afgifte van andere pro-inflammatoire stoffen voorkomt cytokinen Y chemokinen door het stimuleren van immune cellenzoals T-helper 17 (Th17) cellen.
- Guselkumab blokkeert dus de abnormaal verhoogde signalering van de inflammatoire cascades (het kettingreactieproces dat de immuunrespons activeert) die epidermaal afwijkingen, inclusief keratinocyten hyperproliferatie (niet-onderdrukte wondgenezing) en psoriatische plaquevorming.
Hoe wordt guselkumab toegediend?
- Guselkumab wordt toegediend door onderhuids injectie.
- De aanbevolen dosis is 100 mg in week 0, week 4 en daarna elke 8 weken.
- Guselkumab mag niet worden geïnjecteerd op plaatsen waar de huid gevoelig, gekneusd, rood, hard, dik, geschubd, of aangetast door psoriasis.
- Het is bedoeld voor gebruik onder begeleiding en supervisie van een arts.
- Guselkumab kan worden toegediend door een beroepsbeoefenaar in de gezondheidszorg of een patiënt kan zichzelf injecteren na een passende training in subcutane injectietechniek.
- Guselkumab kan het risico op infectie.
- De gemiste dosis moet worden geïnjecteerd zodra dit wordt herinnerd en de volgende dosis moet op het juiste geplande tijdstip worden gegeven.
Evaluatie voorafgaand aan de behandeling voor tuberculose en immunisatie
- De behandeling met guselkumab mag niet worden gestart bij patiënten met een klinisch significante actieve infectie totdat de infectie is verdwenen of afdoende is behandeld.
- Patiënten met een voorgeschiedenis van latent tuberculose moet adequaat worden behandeld voordat guselkumab wordt toegediend, omdat dit een latente tuberculose-infectie kan reactiveren.
- Patiënten mogen tijdens de behandeling met guselkumab niet worden geïmmuniseerd met levende vaccins.
Gebruik in specifieke populaties
Zwangere vrouw
- Er zijn geen gegevens beschikbaar over het gebruik van guselkumab bij zwangere vrouwen, wat erop wijst dat er een geneesmiddelgerelateerd risico bestaat in verband met ernstige aangeboren afwijkingen en miskramen.
- niet nadelig ontwikkelingsgericht Effecten bij nakomelingen van 0 tot 6 maanden oud werden waargenomen bij cynomolgus apen behandeld met guselkumab tot 30 keer de maximaal aanbevolen dosis voor de mens.
- Zie de DermNet NZ-pagina over de veiligheid van medicijnen die tijdens de zwangerschap worden ingenomen.
Moeders en baby's die borstvoeding geven
- Er is geen informatie over de aanwezigheid van guselkumab in moedermelk of de effecten ervan op de zuigeling.
- Bij het voorschrijven van guselkumab aan de moeder moeten de mogelijke risico's en voordelen worden afgewogen.
- Zie de DermNet NZ-pagina over borstvoeding en huid.
Kinderen
De veiligheid en werkzaamheid van guselkumab bij pediatrisch geen patiënten zijn geëvalueerd <18 años.
Oude mensen
Klinische onderzoeken met guselkumab omvatten onvoldoende patiënten van 65 jaar en ouder om te bepalen of zij anders reageren dan jongere proefpersonen.
Patiënten met lever of nier onbekwaamheid
Er zijn geen onderzoeken uitgevoerd om het effect van lever- of nierinsufficiëntie op de farmacokinetiek door guselkumab.
Bijwerkingen van guselkumab
De meest voorkomende Bijwerkingen (≥ 1% van patiënten) gemeld zijn onder andere:
- bovenste luchtwegen infecties
- Hoofdpijn
- Reacties op de injectieplaats
- Artralgie
- Diarree
- Buikgriep
- ringworm infectie
- Herpes simplex infectie.
Geneesmiddelinteracties met Guselkumab
- Er zijn geen gegevens beschikbaar over het vermogen van levende of geïnactiveerde vaccins om een immuunrespons op te wekken bij patiënten die met guselkumab worden behandeld.
- Levende vaccins mogen niet worden gebruikt. gelijktijdig tijdens de behandeling met guselkumab.
- Bevolking farmacokinetisch Analyses hebben uitgewezen dat de gelijktijdig het gebruik van ibuprofen, aspirine of paracetamol heeft geen invloed op de klaring van guselkumab.
- Het effect van geneesmiddelen die worden gemetaboliseerd door hepatisch cytochroom P450 enzymen (bijv. warfarine en ciclosporine) kan worden gewijzigd tijdens gelijktijdige toediening met guselkumab. Dosisaanpassing van deze geneesmiddelen moet worden overwogen.
- De resultaten van een verkennend onderzoek naar geneesmiddeleninteractie bij patiënten met matige tot ernstige psoriasis hebben een laag potentieel voor klinisch relevante geneesmiddelinteracties gesuggereerd voor geneesmiddelen die worden gemetaboliseerd door CYP3A4 (midazolam), CYP2C9 (warfarine), CYP2C19 (omeprazol) en CYP1A2 (cafeïne). ) , maar de mogelijkheid van interactie voor geneesmiddelen die worden gemetaboliseerd door CYP2D6 (metoprolol) kan niet worden uitgesloten.
Contra-indicaties guselkumab
Guselkumab mag niet worden gebruikt bij patiënten die:
- U heeft een infectie die niet weggaat of die terugkomt.
- Nauw contact hebben gehad of gehad met iemand met tbc
- Onlangs een vaccin hebben gekregen of gepland zijn om te worden gevaccineerd
- van plan om zwanger te worden
- Borstvoeding geven of van plan zijn borstvoeding te geven.
Guselkumab is veelbelovend voor plaque psoriasis in fase III-onderzoeken.
- Guselkumab heeft een acceptabel veiligheidsprofiel laten zien en is goed effectiviteit bij de behandeling van matige tot ernstige plaque psoriasis.
- Het is een eersteklas biologische therapie die selectief alleen IL-23 blokkeert, een cytokine dat een sleutelrol speelt bij plaque psoriasis.
- Guselkumab heeft aangetoond hoger resulteert in huidverlichting in vergelijking met adalimumab in vergelijkende analyses.
- Resultaten van klinische onderzoeken hebben ook de werkzaamheid van guselkumab aangetoond bij patiënten die onvoldoende reageerden op behandeling met ustekinumab.
- Een fase III-studie ter evaluatie van guselkumab bij de behandeling van actieve arthritis psoriatica is aan de gang, en een fase III-programma ter evaluatie van de werkzaamheid van guselkumab in vergelijking met secukinumab bij de behandeling van matige tot matige plaque psoriasis is aan de gang.
- Hoewel verdere studies nodig zijn om de veiligheid en werkzaamheid op lange termijn te beoordelen, lijkt guselkumab op basis van de resultaten tot nu toe een veelbelovend medicijn. therapeutisch optie voor matige tot ernstige plaque psoriasis.