Wat is cobimetinib?
Cobimetinib (Cotellic™, Genentech Inc. Californië, VS) is een receptgeneesmiddel dat in combinatie met vemurafenib wordt gebruikt voor de behandeling van patiënten met melanoma.
Cobimetinib kreeg in 2015 goedkeuring van de Amerikaanse Food and Drug Administration (FDA) in de VS. In april 2017 keurde Medsafe cobimetinib goed voor de behandeling van melanoompatiënten in Nieuw-Zeeland.
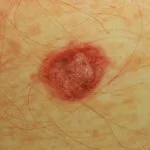
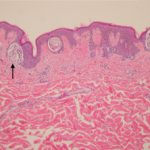
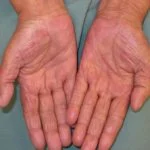
gemetastaseerd melanoom
gemetastaseerd melanoom
gemetastaseerd melanoom
gemetastaseerd melanoom
Wie moet cobimetinib gebruiken?
Cobimetinib, in combinatie met vemurafenib, is geïndiceerd voor de behandeling van patiënten met: inoperabel of metastatisch melanoom, waarbij de kanker die zich heeft verspreid naar andere delen van het lichaam of niet operatief kan worden verwijderd. Een indicator van dit melanoom is een afwijking gen Hij noemde de BRAF V600E of V600K mutatie, die moet worden bevestigd in tumor monsters voordat u met de behandeling begint.
Cobimetinib is niet geïndiceerd voor de behandeling van patiënten met een normaal of wild type. BRAF gen.
Hoe werkt cobimetinib?
Cobimetinib is een kleine molecuul remmer dat blokkeert de MEK enzym, een onderdeel van de kinasecascade in geactiveerd mitogeen eiwit kinaseMAPK) traject. Componenten van de MAPK-routes zijn vaak gemuteerd bij patiënten met kwaadaardige melanoom, in het bijzonder RAF isovorm BRAF. mutaties van BRAF een constitutieve activering van deze signaalroutes veroorzaken, wat kan leiden tot kanker.
Cobimetinib en vemurafenib richten zich op twee verschillende kinasen in de MAPK-route. Klinische onderzoeken hebben aangetoond dat de combinatie van cobimetinib met vemurafenib de overleving verbetert bij melanoompatiënten met de BRAF V600 mutatie.
Hoe wordt cobimetinib toegediend?
Aanbevolen dosis
Cobimetinib is verkrijgbaar in tabletten van 20 mg onder de merknaam Cotellic.
- De aanbevolen dosis is 60 mg eenmaal daags gedurende de eerste 21 dagen van elke cyclus van 28 dagen, voortgezet tot ziekteprogressie of ondraaglijk. toxiciteit komt voor.
- Cobimetinib kan met of zonder voedsel worden ingenomen.
- Als een dosis wordt gemist of als er braken optreedt wanneer de dosis wordt ingenomen, hervat dan de dosering met de volgende geplande dosis.
Vemurafenib (ZELBORAF™) moet elke dag van de cyclus van 28 dagen elke 12 uur worden ingenomen (geen rustperiode). Als u een dosis vemurafenib heeft overgeslagen, moet u deze innemen zodra u eraan denkt. Haal de gemiste dosis niet in als de gemiste dosis binnen 4 uur na de volgende geplande dosis is.
Gebruik van cobimetinib bij specifieke populaties
Zwangere vrouw
Gegevens over het gebruik van cobimetinib bij zwangere vrouwen zijn niet beschikbaar om te informeren over een geneesmiddelgerelateerd risico op ernstige geboorteafwijkingen en miskraam. Op basis van de bevindingen van reproductieonderzoeken bij dieren en het werkingsmechanisme ervan, kan cobimetinib schade aan de foetus veroorzaken. Zwangere vrouwen moeten worden gewaarschuwd voor het mogelijke risico voor de foetus.
Vrouwen die borstvoeding geven
Er is geen informatie over de aanwezigheid van cobimetinib in moedermelk of de effecten ervan op een zuigeling. Bij het voorschrijven van cobimetinib aan de moeder dient rekening te worden gehouden met de mogelijke baten-risicoverhouding. Vrouwen die borstvoeding geven, dienen te worden geadviseerd geen borstvoeding te geven tijdens de behandeling met cobimetinib en gedurende 2 weken na de laatste dosis.
Kinderen
De veiligheid en werkzaamheid van cobimetinib bij kinderen zijn niet geëvalueerd.
Vrouwtjes en mannetjes in de vruchtbare leeftijd
Vrouwelijke patiënten in de vruchtbare leeftijd dienen te worden geadviseerd effectieve anticonceptie te gebruiken tijdens de behandeling met cobimetinib en gedurende 2 weken na de laatste dosis. Op basis van bevindingen bij dieren kan cobimetinib de vruchtbaarheid bij vrouwtjes en mannetjes met voortplantingsvermogen verminderen.
Oude mensen
Klinische onderzoeken met cobimetinib omvatten niet voldoende aantallen mensen van 65 jaar en ouder om te bepalen of zij anders reageren dan jongere proefpersonen.
Personen met lever of nier onbekwaamheid
Er is geen dosisaanpassing van cobimetinib nodig bij patiënten met een lichte (Child-Pugh-score A), matige (Child-Pugh B) of ernstige (Child-Pugh C) leverfunctiestoornis. niet toegewijd farmacokinetiek Er is een proef uitgevoerd bij patiënten met nierinsufficiëntie. Dosisaanpassing wordt niet aanbevolen voor lichte tot matige nierinsufficiëntie (creatinineklaring 30 tot 89 ml/minuut) op basis van de resultaten van de farmacokinetische populatieanalyse. Een aanbevolen dosis voor patiënten met ernstige nierinsufficiëntie is niet vastgesteld.
Wat zijn de mogelijke bijwerkingen van cobimetinib?
Vaak voorkomende bijwerkingen zijn:
- Diarree
- Uitslag
- lichtgevoeligheid
- Misselijkheid
- stomatitis
- Koorts
- alopecia
- trombocytopenie.
Zeldzame maar mogelijk ernstige bijwerkingen zijn onder meer:
- Ernstige diarree die leidt tot uitdroging en nierfalen.
- Rabdomyolyse
- cardiale toxiciteit
- Netvliesloslating
- Embryonale en foetale toxiciteit
- Gewrichtspijn (artralgie).
hepatotoxiciteit
verhogingen in serum aminotransferase en alkalisch fosfatase De spiegels komen vaak voor tijdens behandeling met vemurafenib en komen zelfs vaker voor in combinatie met cobimetinib.
Gevallen van klinisch duidelijk leverletsel met geelzucht Ze zijn gemeld tijdens klinische onderzoeken naar behandeling met cobimetinib en vemurafenib, maar de klinische kenmerken, het beloop en de resultaten van deze episodes zijn niet in detail beschreven.
Het MAPK-pad remmers als een klasse worden ze vaak geassocieerd met vergankelijk serumenzymverhogingen en, zeldzamer, met gevallen van klinisch duidelijke leverbeschadiging, maar de klinische kenmerken zijn niet beschreven en de associatie met cobimetinib is niet duidelijk gedefinieerd.
Het aantal klinisch significante leverbeschadiging en leverfalen geassocieerd met proteïnekinaseremmers is verhoogd bij patiënten met cirrose of leverfalen als gevolg van levertumorbelasting. Het productlabel van cobimetinib beveelt routinematige controle van leverfunctietesten tijdens de behandeling aan.
Verhogingen van serumaminotransferase boven vijf keer de bovengrens van normaal (indien bevestigd) zouden moeten leiden tot tijdelijke opschorting, die permanent zou moeten worden als deze laboratoriumwaarden niet significant verbeteren of binnen een paar weken verdwijnen.
Er lijkt geen kruisreactiviteit te zijn met andere tyrosinekinase ontvanger remmers. In sommige situaties kan het aangewezen zijn om over te schakelen op een andere proteïnekinaseremmer.
Risico op nieuwe kankers
Cobimetinib in combinatie met vemurafenib kan nieuwe huidkankers veroorzaken. Deze kunnen zijn:
- huid geschubd cel carcinoom
- Keratoacanthoma
- basaal cel carcinoom.
Hart problemen
cardiomyopathie, gedefinieerd als symptomatisch en asymptomatisch verminderde ejectie uit de linker ventrikel fractie (LVEF), kan optreden bij cobimetinib.
De veiligheid van cobimetinib is niet vastgesteld bij patiënten met: baseren LVEF die onder de onderste institutionele limiet van normaal of onder de 50% ligt.
De LVEF moet worden beoordeeld voorafgaand aan de start van cobimetinib, 1 maand na de start en daarna elke 3 maanden totdat de behandeling wordt stopgezet. Linksventriculaire gebeurtenissen disfunctie moet worden behandeld door onderbreking, vermindering of stopzetting van de behandeling.
Geneesmiddelinteracties
Cobimetinib wordt in de lever gemetaboliseerd via het cytochroom P450-systeem, voornamelijk CYP3A, en wordt gevoelig op geneesmiddelinteracties met krachtige remmers of inductoren van dit microsomale enzym.
Gelijktijdige toediening van cobimetinib met itraconazol (een sterke CYP3A4-remmer) verhoogde cobimetinib systemisch belichting met 6,7 keer.
Gelijktijdig Het gebruik van cobimetinib en sterke of matige CYP3A-remmers moet worden vermeden. Als kortdurend (14 dagen of minder) gelijktijdig gebruik van matige CYP3A-remmers, waaronder bepaalde antibiotica (bijv. erytromycine, ciprofloxacine) onvermijdelijk is (14 dagen of minder), moet de dosis cobimetinib worden verlaagd van 60 naar 20 mg
Een alternatief voor een sterke of matige CYP3A-remmer moet worden gebruikt bij patiënten die een verlaagde dosis cobimetinib (40 of 20 mg per dag) gebruiken. Na stopzetting van een matige CYP3A-remmer moet cobimetinib worden hervat met de vorige dosis.
Gelijktijdige toediening van cobimetinib met een sterke CYP3A-inductor kan de systemische blootstelling aan cobimetinib met meer dan 80% verlagen en de effectiviteit. Gelijktijdig gebruik van cobimetinib en sterke of matige CYP3A-inductoren, inclusief maar niet beperkt tot carbamazepine, efavirenz, fenytoïne, rifampicine en sint-janskruid, moet worden vermeden.
Contra-indicaties
Cobimetinib moet worden stopgezet in de volgende omstandigheden:
- Geschiedenis van psychische problemen, waaronder zelfmoordgedachten, depressie, angst of stemmingsproblemen.
- Gelijktijdig infectie dat gaat niet weg of komt steeds terug
- Tuberculose (tbc) of nauw contact met iemand met tuberculose
- Onlangs een vaccin ontvangen of gepland om te ontvangen
- van plan om zwanger te worden
- Borstvoeding geven of van plan zijn borstvoeding te geven.