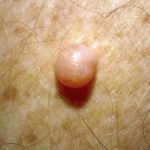
introduzione
Nel luglio 2015, la FDA (Food and Drug Administration) statunitense ha approvato sonidegib (Odomzo®; Novartis, New Jersey, USA) per il trattamento di pazienti adulti con basale cellula carcinoma (BCC).
La Commissione europea ha approvato l'uso di sonidegib per il carcinoma basocellulare nell'agosto 2015. Nel giugno 2016 è stata concessa l'autorizzazione all'immissione in commercio per sonidegib in Svizzera per il trattamento di adulti con carcinoma basocellulare avanzato. Il farmaco è approvato anche in Australia, ma non è ancora disponibile in Nuova Zelanda.
Sonidegib è un inibitore dalla Via del Riccio. Si lega e inibisce Smoothened, una transmembrana proteina partecipa alla trasduzione del segnale Hedgehog, che svolge un ruolo fondamentale nel mantenimento delle cellule staminali e nella riparazione dei tessuti.
Sonidegib è indicato per il trattamento di pazienti adulti con carcinoma a cellule basali (BCC) localmente avanzato che si è ripresentato dopo intervento chirurgico o radioterapia, o coloro che non sono candidati alla chirurgia o alla radioterapia.
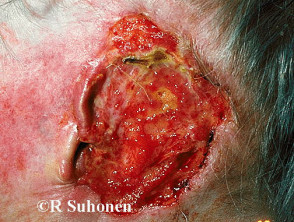
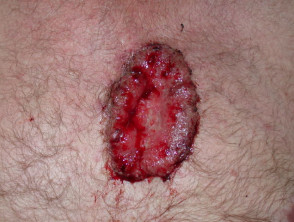
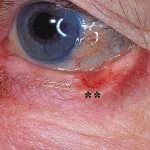
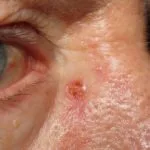
Carcinoma basocellulare avanzato
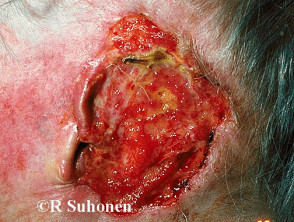
Carcinoma basocellulare avanzato
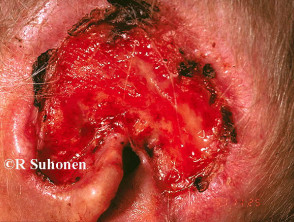
Carcinoma basocellulare avanzato
Carcinoma basocellulare avanzato
Esperienza in studi clinici con sonidegib
- L'approvazione della FDA si è basata su uno studio cardine di fase II (studio BOLT), a doppio cieco, randomizzato, studio non comparativo a due bracci in pazienti con BCC localmente avanzato non suscettibili di terapia locale o metastatico Carcinoma delle cellule basali.
- I pazienti sono stati randomizzati (2:1) a ricevere sonidigib 800 mg (n=151) o 200 mg (n=79) per via orale, una volta al giorno, fino a progressione della malattia o intollerabilità. tossicità.
- Randomizzazione è stato stratificato per stadio di malattia (localmente avanzato o metastatico), malattia BCC localmente avanzata istologia (aggressivi contro non aggressivi) e area geografica.
- I pazienti con BCC localmente avanzato trattati con sonidegib 200 mg (n=66) sono stati seguiti per almeno 12 mesi, salvo interruzione anticipata.
- Il tasso di risposta obiettiva era 58% (95% intervallo di confidenza: 45-70) costituito da 5% (n=3) risposte complete e 53% (n=35) risposte parziali.
- Un'analisi di sensibilità pre-specificata utilizzando una definizione alternativa di risposta completa, definita come almeno una risposta parziale secondo Risonanza magnetica e/o fotografia e senza prova di tumore in biopsia residuo lesione, ha restituito un tasso di risposta completo del 20%.
- Tra i 38 pazienti con una risposta obiettiva, 31 pazienti (82%) hanno risposte continue che vanno da almeno 1,9 a 18,6 mesi.
- il mediano durata della risposta non raggiunta.
- Non c'è stata evidenza di un miglioramento del tasso di risposta obiettiva tra i pazienti con BCC localmente avanzato randomizzati a sonidegib 800 mg al giorno e seguiti per almeno 12 mesi.
- Chemioterapia includeva dacarbazina 1000 mg/m22 ogni 3 settimane o combinazione di carboplatino AUC (area sotto la curva) 6 ogni 3 settimane più paclitaxel 175 mg/m22 ogni 3 settimane.
- il primario L'endpoint era il tasso di risposta obiettiva (ORR) definito come la percentuale di pazienti con risposta tumorale completa o parziale confermata, o riduzione, misurata da un comitato di revisione centrale.
- La valutazione della risposta del tumore si basava su una valutazione composita che integrava le misurazioni del tumore ottenute mediante valutazioni radiografiche mirate. lesioni (secondo RECIST 1.1 o mRECIST), fotografia clinica digitale e istopatologia valutazioni (tramite punch biopsie).
- Tutte le modalità utilizzate devono aver dimostrato l'assenza di tumore per ottenere una valutazione composita della risposta completa.
- La durata della risposta, determinata da una revisione centrale in cieco, è stata una misura di esito secondario chiave.
Reazioni avverse: esperienza in studi clinici
- Reazione avversa I tassi osservati negli studi clinici di un farmaco potrebbero non riflettere i tassi osservati nella pratica clinica perché gli studi clinici sono condotti in condizioni molto variabili.
- La frequenza delle reazioni avverse comuni è stata maggiore nei pazienti trattati con sonidegib 800 mg rispetto a 200 mg.
- Le tabelle 1 e 2 riflettono eventi avversi in >10% di pazienti esposti a sonidegib 200 mg al giorno (79 pazienti con BCC localmente avanzato [n=66] o BCC metastatico [13]).
- I pazienti sono stati seguiti per almeno 18 mesi.
- La durata mediana del trattamento è stata di 11,0 mesi (intervallo da 1,3 a 33,5 mesi).
Muscoloscheletrico e tessuto connettivo disturbi
- Spasmi muscolari 54% (3% Grado 3)
- Mialgia (dolore muscolare) 19% (0)
- Dolore muscoloscheletrico 32 (1%)
Pelle e sottocutaneo disturbi dei tessuti
- Alopecia 53% (0 gradi 3)
- Prurito 10% (0)
Disturbi del sistema nervoso
- Disgeusia (gusto anormale) 46% (0 Grado 3)
- Cefalea 15% (1%)
Reazioni del sito di somministrazione
- Dolore 14% (1% Grado 3)
Disordini gastrointestinali
- Nausea 39% (1% Grado 3)
- Diarrea 32% (1%)
- Dolore addominale 18% (0)
- Vomito 11% (1%)
Metabolismo e nutrizione
- Diminuzione dell'appetito 23% (1% Grado 3)
laboratorio chiave anomalie
- È aumentato siero creatina chinasi (muscolo enzima) 61% (8% Grado 3-4)
- iperglicemia 51% (4%)
- È aumentato alanina aminotransferasi 43% (13%)
- È aumentato aspartato aminotransferasi 19% (4%)
- Aumento dell'amilasi 16% (1%)
- Anemia 32% (0)
- Linfopenia (ridotto linfociti) 28% (3%)
Follow-up a lungo termine: esperienza negli studi clinici
- Sonidegib ha mostrato un'attività antitumorale continua senza nuovi problemi di sicurezza nei pazienti con carcinoma basocellulare avanzato, sulla base dei risultati del follow-up a 30 mesi dello studio cardine BOLT presentato al meeting annuale ASCO 2016.
- L'outcome primario era il tasso di risposta obiettiva.
- Gli endpoint secondari includevano la durata della risposta, la risposta completa, la sopravvivenza libera da progressione, la sopravvivenza globale e la sicurezza.
- Al follow-up di 30 mesi, i pazienti con BCC localmente avanzato avevano un tasso di risposta obiettiva di 56% e 45% rispettivamente con le 2 dosi dello studio di 200 mg e 800 mg di sonidegib.
- Tra i pazienti con BCC metastatico, i tassi di risposta obiettiva alle dosi più basse e più alte erano rispettivamente 8% e 17%.
- Nel gruppo localmente avanzato, il tasso di risposta completa era 5%, il tasso di risposta parziale era 52% e il tasso di malattia stabile era 35%.
- La durata mediana della risposta è stata di 26,1 mesi, la PFS mediana è stata di 22,1 mesi e il tasso di sopravvivenza globale a 2 anni è stato di 93% (95% CI, 80-98).
- Nei pazienti con BCC metastatico trattati con la dose di 200 mg, non ci sono state risposte complete, il tasso di risposta parziale è stato 8%, il tasso di malattia stabile 85% e il tasso di progressivo malattia era 0.
- La durata mediana della risposta è stata di 24 mesi, la PFS mediana è stata di 13,1 mesi (95% CI, 5,6-33,1) e il tasso di sopravvivenza globale a 2 anni è stato di 69% (95% CI, 31-89).
- Tutti i pazienti che hanno ricevuto la dose da 800 mg e 97.5% dei pazienti che hanno ricevuto la dose da 200 mg hanno manifestato almeno 1 evento avverso.
- I tassi di eventi avversi di grado 3/4 (43% rispetto a 64%) e di eventi avversi gravi (20% rispetto a 39%) erano inferiori con la dose da 200 mg rispetto alla dose da 800 mg.
- Tra i 79 pazienti che hanno ricevuto sonidegib 200 mg, gli eventi avversi di tutti i gradi più comuni sono stati spasmi muscolari (54%), alopecia (49%), disgeusia (44%), nausea (39%), diarrea (32%). ) e perdita di peso (30%).
- Gli eventi avversi di grado 3/4 più comuni sono stati aumento della creatinina chinasi (7%), diminuzione del peso (5%), spasmi muscolari (3%).
Direzioni future per sonidegib
- Sonidegib ha mostrato efficacia nel trattamento di non resecabile carcinoma basocellulare localmente avanzato e metastatico.
- Le tossicità identificate sono gestibili e reversibili con l'interruzione del trattamento.
- Tuttavia, sonidegib non è stato ancora confrontato con altre terapie approvate con inibitori della via del riccio per il carcinoma a cellule basali, come vismodegib.
- Sulla base dei risultati presentati all'ASCO Annual Meeting 2016, un ampio studio (studio STEVIE; n=1.215) ha confermato i benefici di vismodegib per il carcinoma basocellulare.
- L'accettabile profilo beneficio-rischio di sonidegib, insieme alla scarsità di opzioni terapeutiche, rende sonidegib un'opzione emergente per il trattamento di adulti con BCC localmente avanzato che si è ripresentato dopo intervento chirurgico o radioterapia, o in coloro che non sono candidati a intervento chirurgico o radioterapia. terapia.
- La continua approvazione di sonidegib per il trattamento del carcinoma a cellule basali dipenderà dalla verifica del beneficio clinico negli studi di conferma.