introduzione
Nel febbraio 2017, il trattamento biologico brodalumab (Siliq ™; Valeant Pharmaceuticals, NJ, USA) ha ricevuto l'approvazione dalla Food and Drug Administration (FDA) statunitense per il trattamento della psoriasi nei pazienti adulti. che non hanno risposto ad altri trattamenti.
Valeant prevede di iniziare a commercializzare e commercializzare brodalumab negli Stati Uniti nella seconda metà del 2017.
A causa del rischio osservato di ideazione e comportamento suicidario, l'etichettatura di brodalumab include un avviso in scatola e il farmaco è disponibile solo attraverso un programma limitato nell'ambito del programma REMS (Risk Assessment and Mitigation Strategies) della FDA. Di seguito sono riportati importanti requisiti del programma.
- I medici prescrittori devono essere certificati con il programma REMS e consigliare i pazienti sul rischio di ideazione e comportamento suicidari.
- I pazienti con sintomi di depressione nuovi o in peggioramento o tendenze suicide devono essere indirizzati a un professionista della salute mentale, a seconda dei casi.
- I pazienti dovrebbero cartello un modulo di accordo tra il paziente e il medico prescrittore ed essere consapevoli della necessità di consultare un medico se sperimentano pensieri o comportamenti suicidi nuovi o in peggioramento, sentimenti di depressione, ansia o altri sbalzi d'umore.
- Anche le farmacie devono essere certificate con il programma REMS e dovrebbero dispensare brodalumab solo ai pazienti autorizzati a ricevere il farmaco.
Non è stata stabilita un'associazione causale tra il trattamento con brodalumab e un aumentato rischio di ideazione e comportamento suicidari.
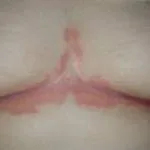
Psoriasi cronica a placche
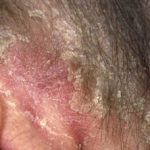
Psoriasi del cuoio capelluto
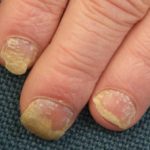
Psoriasi delle mani
Psoriasi cronica a placche
A cosa serve brodalumab?
Brodalumab è usato per trattare pazienti adulti con malattia da moderata a grave. targa psoriasi che sono candidati per sistemico terapia o fototerapia e non hanno risposto o hanno smesso di rispondere ad altre terapie sistemiche.
È raccomandato per i candidati per i quali la terapia sistemica o la fototerapia non è riuscita a fornire un trattamento o risultati adeguati.
Come funziona brodalumab?
Brodalumab è un monoclonale immunoglobuline G2 (IgG2) anticorpo che inibisce infiammatorio reazioni e si lega selettivamente a ricevitore di interleuchina 17 (IL-17), a citochina cosa inizia infiammazione.
Il recettore IL-17 è a proteina espresso sulla superficie cellulare ed è un componente dei complessi recettoriali utilizzati da più famiglie di IL-17 citochinecome IL-17A, IL-17F, IL-17C, IL-17A / F eterodimero e IL-25. Il blocco del recettore IL-17 inibisce le risposte di IL-17 indotte dalle citochine, incluso il rilascio di pro-infiammatorio citochine e chemochine associato con il Patogenesi della psoriasi.
Come viene somministrato brodalumab?
Brodalumab viene somministrato per via sottocutanea. Ogni siringa preriempita (1,5 ml) contiene 210 mg di brodalumab ed è esclusivamente monouso.
- La dose raccomandata di brodalumab è di 210 mg somministrati da sottocutaneo iniezione alle settimane 0, 1 e 2, seguita da 210 mg ogni 2 settimane.
- Se non è stata ottenuta una risposta adeguata dopo 12-16 settimane di trattamento, il trattamento con brodalumab deve essere interrotto.
- Brodalumab non deve essere iniettato in aree dove la pelle è sensibile, livida, arrossata, dura, spessa, squamosoo affetti da psoriasi.
- Brodalumab è controindicato nei pazienti con malattia di Crohn perché il farmaco può peggiorare la malattia.
- Pazienti con una storia di latente La tubercolosi deve essere trattata prima della somministrazione di brodalumab, che può riattivare la tubercolosi latente. infezione.
L'uso di brodalumab in popolazioni specifiche
Donne incinte
Non sono disponibili dati sull'uso di brodalumab in donne in gravidanza per informare i medici del rischio associato al farmaco di gravi difetti alla nascita e aborto spontaneo.
Non negativo evolutivo Sono stati osservati effetti in scimmie gravide dopo somministrazione sottocutanea di brodalumab fino a 26 volte la dose massima raccomandata nell'uomo. (Vedere Sicurezza dei medicinali presi durante la gravidanza per ulteriori informazioni.)
Donne che allattano
Non sono disponibili informazioni sulla presenza di brodalumab nel latte materno o sui suoi effetti sul lattante. Il potenziale rischio-beneficio deve essere considerato quando si prescrive brodalumab a una madre che allatta. (Vedi Allattamento e pelle).
Bambini
La sicurezza e l'efficacia di brodalumab non sono state valutate in pediatrico pazienti.
Anziani
Gli studi clinici con brodalumab non hanno incluso un numero sufficiente di soggetti di età pari o superiore a 65 anni per determinare se gli anziani risponderanno in modo diverso ai giovani.
Individui con epatica o renale disabilità
Non sono stati condotti studi per valutare l'uso di brodalumab in pazienti con funzionalità epatica o renale compromessa.
Quali sono i rischi di brodalumab?
Eventi avversi
Il più comune Reazioni avverse (≥ 1% dei pazienti) riportati con brodalumab includono:
- Artralgia (dolori articolari)
- Mal di testa
- Fatica
- Diarrea
- Orofaringea dolore (mal di gola)
- Nausea
- Mialgia (Dolore muscolare)
- Reazioni al sito di iniezione
- Influenza
- Neutropenia (basso numero di globuli bianchi)
- Funghi infezioni (come tigna).
Le seguenti reazioni avverse gravi sono state riportate negli studi clinici in pazienti trattati con brodalumab:
- Ideazione e comportamento suicidari
- Infezioni gravi come i criptococchi meningite
- Riattivazione latente della tubercolosi
- Esacerbazione della malattia di Crohn.
Interazioni farmacologiche
Non sono disponibili dati sulla capacità dei vaccini vivi o inattivi di provocare una risposta immunitaria nei pazienti in trattamento con brodalumab. I vaccini vivi non devono essere utilizzati durante il trattamento con brodalumab.
L'effetto dei farmaci metabolizzati attraverso il citocromo epatico P450 enzimi (come warfarin e ciclosporina) possono essere alterati durante simultaneo somministrazione con brodalumab. Si dovrebbe prendere in considerazione la modifica delle dosi di questi farmaci.
Controindicazioni
Brodalumab è controindicato nelle persone che:
- Hai una storia di problemi mentali, inclusi pensieri suicidi, depressione, ansia o problemi di umore.
- Avere infezioni ricorrenti
- Hai la tubercolosi o sei stato a stretto contatto con qualcuno affetto da tubercolosi.
- Hai ricevuto di recente o stai pianificando di ricevere una vaccinazione.
- Stai pianificando una gravidanza
- Stai attualmente allattando al seno o stai pianificando di allattare.
Quali sono le prospettive per il trattamento con brodalumab?
Brodalumab ha mostrato un profilo di sicurezza accettabile e buono efficacia nel trattamento della psoriasi a placche da moderata a grave. Fornisce un'importante nuova terapia nel trattamento della psoriasi dove rimane un significativo bisogno insoddisfatto di nuovi agenti con nuovi meccanismi di azione, una rapida insorgenza dell'effetto e una migliore e sostenuta clearance totale della pelle, supportando una Maggiore aderenza del paziente e riduzione al minimo dei problemi di sicurezza specifici del farmaco.
Tuttavia, le attuali prove per brodalumab non sono sufficienti per confermare il mantenimento di questi risultati a lungo termine.