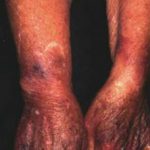
introduzione
Nell'agosto 2018, la Food and Drug Administration (FDA) statunitense ha approvato lanadelumab (nome commerciale Takhzyro™) per la prevenzione della ereditario angioedema attacchi in pazienti ≥ 12 anni. Questo farmaco è stato valutato dalla FDA nell'ambito della sua revisione prioritaria, che è riservata ai farmaci che rappresentano miglioramenti significativi nella sicurezza o efficacia nel trattamento di malattie gravi.
Lo studio HELP
Lo studio HELP era multicentrico, randomizzato, doppio cieco, placebo- Studio controllato a gruppi paralleli su 125 individui (115 adulti e 10 adolescenti), di età pari o superiore a 12 anni, con angioedema ereditario sintomatico di tipo I o II.
Progettazione dello studio
I pazienti sono stati randomizzati a ricevere lanadelumab alle seguenti dosi:
- Lanadelumab 150 mg ogni 4 settimane (q4w) (n = 28)
- Lanadelumab 300 mg ogni 4 settimane (q4w) (n = 29)
- Lanadelumab 300 mg ogni 2 settimane (q2w) (n = 27)
- Placebo per 26 settimane (n = 41).
precedente a randomizzazione, i pazienti di età pari o superiore a 18 anni dovevano completare uno studio a lungo termine di 2 settimane. profilassi periodo di riposo (sospensione di qualsiasi farmaco usato per prevenire l'angioedema). Tutti i pazienti sono quindi entrati in un periodo di rodaggio di 4 settimane prima dell'arruolamento nello studio per determinare il base tasso di attacco di angioedema. I pazienti con uno o più attacchi di angioedema confermati dallo sperimentatore durante il periodo di run-in di 4 settimane erano eleggibili per l'inclusione nello studio e la randomizzazione. il primario L'endpoint di efficacia era il tasso di attacchi confermati dallo sperimentatore durante il periodo di trattamento (dal giorno 0 al giorno 182).
il metà I tassi di attacco mensili per i diversi gruppi di trattamento al basale durante il periodo di rodaggio sono stati:
- Lanadelumab 150 mg ogni 4 settimane: 3.2
- Lanadelumab 300 mg ogni 4 settimane: 3,7
- Lanadelumab 300 mg ogni 2 settimane: 3,5
- Placebo 4.
I risultati lo hanno dimostrato sottocutaneo Le iniezioni ogni 2 o 4 settimane hanno ridotto significativamente il numero mensile di attacchi in tutti e tre i bracci di trattamento con lanadelumab rispetto al placebo (P <0,001). A 300 mg cada 2 semanas, lanadelumab redujo el número medio de ataques de angioedema por mes en un 87% en comparación con placebo (ajustado P <0,001).
Durante il periodo di trattamento, il numero medio di attacchi al mese è stato:
- Lanadelumab 150 mg ogni 4 settimane: 0,48
- Lanadelumab 300 mg ogni 4 settimane: 0,53
- Landelumab 300 mg ogni 2 settimane: 0,26
- Placebo: 1,97.
Rispetto al placebo, le differenze medie nel tasso di attacco al mese sono state:
- Lanadelumab 150 mg ogni 4 settimane: -1,49 (intervallo di confidenza 95% [CI]: -1,90, -1,08; P <0,001)
- Lanadelumab 300 mg ogni 4 settimane: -1,44 (IC 95%: -1,84, -1,04; P <0,001)
- Lanadelumab 300 mg ogni 2 settimane: -1,71 (IC 95%: -2,09, -1,33: P <0,001).
La riduzione media del tasso di attacco di angioedema ereditario è stata costantemente più elevata nei gruppi di trattamento con lanadelumab rispetto al placebo, indipendentemente dalla storia al basale di precedente profilassi a lungo termine. laringeo attacchi o tasso di attacco durante il periodo di rodaggio.
Altri endpoint esplorativi predefiniti nello studio HELP includevano la percentuale di pazienti che erano liberi da crisi durante l'intero periodo di trattamento di 26 settimane e la percentuale di pazienti che avevano raggiunto riduzioni della soglia nei tassi di attacco di angioedema (≥ 50%, ≥ 70%, ≥ 90%) rispetto alla linea di base.
È stata osservata una riduzione di 50% o superiore del tasso di attacco di angioedema in 100% pazienti trattati con lanadelumab 300 mg ogni 2 settimane o ogni 4 settimane e 89% pazienti trattati con lanadelumab 150 mg ogni 4 settimane rispetto ai 32% dei pazienti trattati con placebo.
È stata osservata una riduzione pari o superiore a 70% del tasso di attacco di angioedema in 89%, 76% e 79% nei pazienti trattati rispettivamente con lanadelumab 300 mg ogni 2 settimane, 300 mg ogni 4 settimane e 150 mg ogni 4 settimane, rispetto al 10% del placebo pazienti.
Una riduzione di 90% o superiore nel tasso di attacco di angioedema è stata osservata in 67%, 55% e 64% di pazienti trattati con lanadelumab 300 mg ogni 2 settimane, 300 mg ogni 4 settimane e 150 mg ogni 4 settimane, rispettivamente, rispetto al 5% di i pazienti con placebo.
Rispetto al 2% dei pazienti nel gruppo placebo, la percentuale di pazienti senza crisi durante l'intero periodo di trattamento di 26 settimane è stata:
- 44% nel braccio lanadelumab 300 mg ogni 2 settimane
- 31% nel braccio lanadelumab 300 mg ogni 4 settimane
- 39% nel braccio lanadelumab 150 mg ogni 4 settimane.
Limiti dello studio
C'erano relativamente pochi pazienti in ciascun gruppo di trattamento. Lo studio HELP è stato limitato a 26 settimane e non è possibile trarre conclusioni sulla sicurezza e l'efficacia a lungo termine.
Qualità della vita legata alla salute
L'Angioedema Quality of Life Questionnaire (AE-QoL) misura l'impatto dell'angioedema riferito dal paziente in un periodo di 4 settimane. ricorda periodo in quattro domini: paura/vergogna, funzionamento, affaticamento/umore e nutrizione.
Tutti i gruppi di trattamento nello studio HELP hanno mostrato un miglioramento del punteggio totale AE-QoL rispetto al placebo.
La percentuale di pazienti che ha ottenuto un miglioramento clinicamente significativo nel punteggio totale AE-QoL rispetto a 37% di pazienti nel gruppo placebo è stata:
- 65% nel braccio lanadelumab 150 mg ogni 4 settimane (odds ratio vs placebo = 3,2 [IC 95%: 1,1-9,2])
- 63% nel braccio lanadelumab 300 mg ogni 4 settimane (2,9 [IC 95%: 1,1-8,1])
- 81% nel gruppo lanadelumab 300 mg q2w (7,2 [IC 95%: 2,2-23,4]).
Alla settimana 26, i pazienti hanno riportato un miglioramento clinicamente significativo (riduzione di 6 punti) in tutti i domini del punteggio totale AE-QoL. In tutti i bracci di trattamento con lanadelumab rispetto al placebo a 26 settimane, i pazienti hanno riportato:
- Meno paura e vergogna per attacchi imprevedibili (variazione media dei minimi quadrati rispetto al basale di -18,8 [deviazione standard (DS) 23,7] con lanadelumab vs -9 [DS, 24,0] con placebo)
- Meno deterioramento della capacità di lavorare, socializzare e svolgere altre attività fisiche (-29,3 [22,9] vs. -5,4 [22,7])
- Meno fatica durante il giorno e sonno migliore durante la notte (-13 [23,1] vs -1,8 [23,3])
- Meno restrizioni su cibi e bevande (-17 [22,3] vs -0,5 [22,5]).
Eventi avversi
Il più comunemente osservato reazione avversa associate a lanadelumab nello studio HELP sono state reazioni al sito di iniezione, tra cui dolore al sito di iniezione, eritemae lividi nel sito di iniezione. Queste reazioni al sito di iniezione si sono verificate in più di 1 paziente su 10.
Altro Reazioni avverse osservato con una frequenza inferiore (≥ 1/100 to <1>
- Ipersensibilità
- Vertigini
- Maculopapulare (morbilliform) eruzione
- Mialgia
- È aumentato alanina transaminasi e aspartato transaminasi.
Bambini
La sicurezza di lanadelumab è stata valutata in un sottogruppo di 23 pazienti di età compresa tra 12 e 17 anni. I risultati di questa analisi di sottogruppo erano coerenti con i risultati complessivi dello studio per tutti i pazienti.
immunogenicità
Il trattamento con lanadelumab è stato associato a sviluppo di antidroga emergenti dal trattamento anticorpi in 10 su 84 pazienti (11.9%). Tutto anticorpo Titoli erano bassi e non hanno cambiato il farmacocinetica e farmacodinamico caratteristiche di lanadelumab o risposta clinica.
Estensione dello studio HELP
La sicurezza e l'efficacia a lungo termine di lanadelumab come profilassi per prevenire attacchi di angioedema ereditario sono state valutate in uno studio Aperto Estensione dello studio HELP.
Questo studio ha arruolato sia pazienti che hanno completato lo studio HELP in doppio cieco ("pazienti ritornati"; n=109) sia pazienti che non hanno partecipato allo studio in doppio cieco, che comprendeva pazienti che potevano o meno aver utilizzato un altro profilattico trattamento e che avevano un tasso di attacco al basale storico di più di un attacco ogni 12 settimane ("pazienti senza inversione"; n = 103).
I pazienti che si sono capovolti hanno ricevuto una singola dose da 300 mg di lanadelumab il giorno 0 e la seconda dose dopo il primo attacco di angioedema confermato del paziente. Successivamente, lanadelumab è stato somministrato ogni 2 settimane.
I pazienti senza reinversione hanno ricevuto lanadelumab 300 mg ogni 2 settimane indipendentemente dal primo attacco. Tutti i pazienti hanno ricevuto l'ultima dose il giorno 350 (massimo 26 dosi), seguita da un follow-up di 4 settimane.
I risultati provvisori dell'estensione in aperto dello studio HELP hanno rilevato che il trattamento con lanadelumab era generalmente ben tollerato e coerente con il suo profilo di sicurezza osservato in precedenza. Al momento dell'analisi ad interim, i pazienti erano stati esposti a lanadelumab per una media di 8,21 (DS, 2,17) mesi e continuavano a sperimentare una riduzione degli attacchi di angioedema ereditario.
Qual è il potenziale futuro di lanadelumab?
L'angioedema ereditario è una malattia potenzialmente letale che si traduce in una sostanziale diminuzione della qualità della vita.
- Lanadelumab ha un nuovo meccanismo d'azione e può essere di beneficio per i pazienti il cui angioedema non è controllato in modo ottimale da altri farmaci.
- La diminuzione del tasso di attacco e, in alcuni casi, l'eliminazione virtuale di acuto Attacchi: è probabile che riduca l'ansia e lo stress da attacchi futuri e consenta una maggiore libertà per coloro che partecipano ad attività sportive o sociali e una maggiore produttività sul lavoro.
- Il trattamento sottocutaneo per la profilassi può ridurre il carico e la complessità della somministrazione rispetto alla somministrazione endovenosa.
- I pazienti riferiscono che la capacità di autosomministrare la propria terapia può portare a un maggiore senso di controllo sulla malattia, una maggiore capacità di condurre una vita normale e un onere ridotto per gli operatori sanitari.
- Nelle aree in cui l'accesso alle cure mediche o alla terapia su richiesta è limitato, la terapia profilattica a lungo termine potrebbe salvare vite umane.
- Tieni presente che le nuove terapie biologiche spesso hanno problemi di sicurezza molto tempo dopo la loro introduzione sul mercato che non sono stati rilevati negli studi di pre-approvazione.
- Sono necessari ulteriori studi per confermare l'efficacia e la sicurezza a lungo termine di lanadelumab.