Wat is het Epstein-Barr-virus?
Het Epstein-Barr-virus (EBV), ook bekend als humaan herpesvirus 4 (HHV-4), is een van de acht bekende lymfotrope herpesvirussen [1].
- EBV veroorzaakt meestal infectieuze mononucleosis, ook bekend als glandulair koorts, die wordt gekenmerkt door koorts, keelpijn en lymfadenopathie [2].
- De meeste mensen worden gedurende de eerste decennia van hun leven blootgesteld aan EBV asymptomatisch [23]. Na de primair infectie, EBV blijft latent Ter nagedachtenis B-cellenen voor de meeste mensen heeft het geen grote gevolgen voor de gezondheid. [4].
- In sommige gevallen kan EBV de transformatie van B-cellen versterken (de effectiviteit ervan verhogen) en a lymfoproliferatief wanorde.
Welke is de pathogenese van EBV-infectie?
De pathogenese van EBV verloopt volgens het volgende proces [2].
- EBV infecteert eerst epitheel van orofarynx (achterkant van de keel) en speeksel- klieren en komt vrij uit deze cellen.
- Het virus infecteert vervolgens nabijgelegen B-cellen, hetzij rechtstreeks in de amandelen. crypten (zakken of plooien) of na contact met de epitheel cellen.
- Circulerende geïnfecteerde B-cellen verspreiden zich vervolgens via de bloedbaan.
- de proliferatie van EBV-geïnfecteerde B-cellen leidt tot een vergroting van lymfoïde stoffen, incl lymfe klieren.
- B-cellen infecteren elk reagens T-cellen met degenen waarmee ze in contact komen.
- Het virus wordt van persoon op persoon overgedragen via orale afscheidingen.
Wat zijn EBV-geassocieerde lymfoproliferatieve aandoeningen?
EBV-geassocieerde lymfoproliferatieve aandoeningen zijn zeldzaam; waarvan de criteria zijn:
- Eén of meer soorten lymfoïde cellen die zijn geïnfecteerd met EBV
- Geïnfecteerde lymfoïde cellen kunnen zich overmatig delen en leiden tot ontwikkelen van een goedaardig stoornis of een maligniteit [5]
- EBV-geassocieerde maligniteiten omvatten B-cellen lymfoom, T-cel lymfomen en niet-lymfoproliferatieve kankers, nasofaryngeaal en maag carcinoom [2].
EBV-geassocieerde lymfoproliferatieve aandoeningen kunnen optreden als gevolg van latentie deregulering met:
- Humaan immunodeficiëntievirus (hiv) infectie en verworven immunodeficiëntie syndroom (AIDS)
- Andere vormen van immunodeficiëntie
- Immunosuppressivum therapie na stevig Orgaan transplantatie
- Leeftijdsgebonden immunologische veroudering (verslechtering van het immuunsysteem als gevolg van leeftijd) [4,6].
Hoe worden EBV-lymfoproliferatieve aandoeningen geclassificeerd?
De classificatie van EBV-geassocieerde lymfoproliferatieve aandoeningen is gebaseerd op de afstammingslijn van de doelcellen, B-, T- en natural killer (NK)-cellen. [7].
EBV-geassocieerde B-cel lymfoproliferatieve aandoeningen omvatten [7]:
- Burkitt-lymfoom
- Klassiek Hodgkin-lymfoom
- Versturen-transplantatie lymfoproliferatieve aandoening
- HIV-geassocieerde lymfoproliferatieve aandoeningen
- Lymfoproliferatieve aandoeningen gerelateerd aan andere histotypes (weefselsoorten afkomstig van de groei van a tumor) [7].
EBV-geassocieerde T- en NK-cellymfoproliferatieve aandoeningen omvatten [7]:
- randapparatuur T-cellymfoom
- chronisch actieve EBV-infectie van T-cel- en NK-celtypen (met huid Y systemisch vormen)
- Angioimmunoblastisch T-cellymfoom
- extranodaal Nasaal T/NK-cellymfoom.
EBV is directer betrokken bij de laatste twee typen [7].
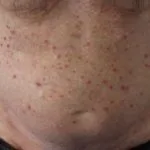
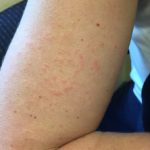
Wat zijn cutaan demonstraties van lymfoproliferatieve aandoeningen geassocieerd met EPV?
De huidkenmerken van EBV-geassocieerde lymfoproliferatieve aandoeningen komen voornamelijk voort uit geïnfecteerde T-cellen of NK cellen. Deze huidmanifestaties worden gezien bij:
- Extranodaal NK/T-cellymfoom [1]
- EBV-positief mucocutaan ontstoken (EBV-MCU) [5]
- lymfomatoïde granulomatose
- Plasmablastisch lymfoom (PBL) [8].
Extranodaal NK/T-cellymfoom
Volgens de huidige classificatie van hematolymfoïde tumoren van de Wereldgezondheidsorganisatie (WHO) is extranodale NK/T-cel Lymfoom is een zeldzame maar uiterst agressieve vorm van lymfoom. [7]. De meeste patiënten met dit type lymfoom vertonen cellulitis of een zweer in het gezicht. [8].
De subcategorieën zijn gebaseerd op hun anatomische deelnamelocaties. [8]:
- 'Nasaal' NK/T-cellymfoom treft meestal het bovenste deel van het spijsverteringskanaal
- 'Nasaal' NK/T-cellymfoom tast de huid aan, zachte stof, maagdarmkanaal en testikels.
Wanneer extranodaal NK/T-cellymfoom zich aanvankelijk manifesteert met huidsymptomen, staat dit bekend als primair cutaan extranodaal NK/T-cellymfoom. Nasaal NK/T-cellymfoom kan zich ook voordoen met metastase [9].
Extranodaal T/NK-cellymfoom van het nasale type omvat meestal knobbeltjesen minder vaak ulceratie in de buik en ledematen [10]. Nasaal T/NK-cellymfoom is klinisch minder agressief en meer gelegen dan het nasale type.
De diagnose van extranodaal NK/T-cellymfoom hangt af van de stadiëring ervan en omvat het voltooien van de volgende onderzoeken [9]:
- Flexibele neusbakendoscopie met biopsieën om de betrokkenheid van de neus te evalueren
- Beenmerg biopsie
- Connecticut onderzoek van borst, buik en bekken
- Huidbiopsie van elke verdachte huid. blessure.
histologischwordt extranodaal NK/T-cellymfoom gekenmerkt door EBV-positiviteit atypisch lymfoïde cytotoxisch infiltreren, vasculair vernietiging en weefsel necrose (zie DermNet NZ-pagina over extranodaal NK/T-cellymfoom, nasaal type, pathologie).
Behandeling van extranodaal NK/T-cellymfoom is afhankelijk in zijn enscenering [9].
- systemisch chemotherapie wordt doorgaans aangeboden.
- Radiotherapie Het is nuttig bij patiënten met ziektestadium I of II die beperkt is tot de neusholte.
- antiviraal De therapie wordt toegepast bij patiënten met een hoge EBV-last.
- Allogene hematopoëtische stamceltransplantatie kan worden overwogen.
- monoklonaal antistoffen Ze worden onderzocht.
Mucocutane zweer positief voor het Epstein-Barr-virus
EBV-MCU is toegevoegd aan de WHO-classificatie van 2016 en is een gelokaliseerde aandoening waar geen sprake van is lymfeklierenbeenmerg, lever of milt. Het presenteert zichzelf meestal als een pijnlijke eenling, nou jaafgebakend zweer in de orofarynx, huid of maag-darmkanaal en kan gepaard gaan met gewichtsverlies [5].
Predisponerende factoren voor EBV-MCU zijn onder meer:
- Behandeling met immunosuppressiva [11]:
- Methotrexaat
- Azathioprine
- Tacrolimus
- mycofenolaat
- Tumornecrosefactor alfa remmers
- Huidig steroïden
- Leeftijdsgebonden immunosenescentie
- Primaire immuundeficiënties [3].
De pathogenese van EBV-MCU correleert met een verminderde populatie T-cellen in immunosuppressie patiënten, wat resulteert in de proliferatie van beperkte klonen van EBV-specifieke T-cellen in het lichaam. Dit leidt tot gelokaliseerde lymfoproliferatie, veroorzaakt door EBV, omdat het immuunsysteem het virus alleen in een slapende toestand kan houden. [elf].
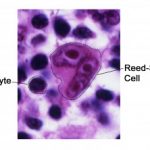
De diagnose werkte want EBV-MCU impliceert in het algemeen histologisch evaluatie met immunohistochemie. De virale lading van EBV is meestal negatief. Histologisch gezien is de verwondingen zijn opgebouwd uit infiltranten van lymfocyten, plasma cellen, histiocytenY eosinofielen, met grote atypische B-celontploffingen die lijken op Reed-Sternberg Hodgkin-cellen. Als gevolg van de histologische kenmerken die vergelijkbaar zijn met die van andere B-cellen proliferatief kankers, verkeerde diagnoses van klassiek of Hodgkin-lymfoom diffuus groot B cel lymfoom is opgetreden [6].
Het ziekteverloop van EBV-MCU neemt doorgaans toe en af en is relatief goedaardig. Patiënten kunnen spontaan refereren of een volledige klinische respons hebben op een vermindering van immunosuppressieve therapieën. In sommige gevallen is dat echter wel het geval aanhoudend invaliderend beloop dat agressieve therapie vereist [3,11].
Behandelingsopties omvatten:
- Monoklonale antilichamen zoals die gericht tegen CD20 antilichaam therapie (bijv. rituximab) of CD30-gerichte antilichaamtherapie (bijv. brentuximab)
- Lokale radiotherapie
- Lokale chirurgische ingreep excisie
- Systemische chemotherapie
- Combinatietherapie.
lymfomatoïde granulomatose
Lymfomatoïde granulomatose is een zeldzame aandoening waarbij sprake is van een overproductie van abnormale B-cellen die zijn geïnfecteerd door EBV. [12]. De cellen infiltreren en hopen zich op in verschillende weefsels van het lichaam.
De symptomen van lymfomatoïde granulomatose variëren afhankelijk van de aangetaste organen.
- Lymfomatoïde granulomatose van de longen veroorzaakt kortademigheid, hoesten en pijn op de borst.
- Andere plaatsen die worden beïnvloed door lymfomatoïde granulomatose zijn het centrale zenuwstelsel, de nieren, de lever en de huid.
- Er kunnen systemische symptomen optreden, zoals ongemak, koorts en gewichtsverlies.
Cutane lymfomatoïde granulomatose kan zich voordoen met [12]:
- Vlekken of pleisters
- papels of platen
- onderhuids of dermaal knobbeltjes
- Ulceratie.
Biopsie van lymfomatoïde granulomatose vertoont meestal een infiltraat van atypische B-cellen polymorf T-cellen, met ontsteking Y necrotisch brandpunten in lymfoïde cellen [13]. Een biopsie is niet altijd betrouwbaar, omdat de karakteristieke abnormale cellen mogelijk ontbreken.
De behandeling van lymfomatoïde granulomatose hangt af van het aantal EBV-positieve B-cellen en de mate van necrose. [12]. Sommige patiënten kunnen spontaan genezen, maar de meeste zullen een behandeling met interferon-alfa-2b of een combinatiechemotherapie met rituximab nodig hebben.
plasmablastisch lymfoom
PBL is een zeldzaam maar agressief subtype van diffuus grootcellig B-cellymfoom [14]. Het wordt vaak geassocieerd met onderliggende immunosuppressie bij patiënten met HIV of een solide orgaantransplantatie, maar PBL kan ook immunocompetente patiënten treffen. [vijftien]. Veel gevallen van PBL worden in verband gebracht met EBV, wat belangrijk is therapeutisch transcendentie [14]. Sommige onderzoeken hebben gemeld dat EBV-positiviteit de uitkomst niet voorspelt, terwijl andere hebben gemeld dat het een betere uitkomst aangeeft voorspelling [16].
El PBL tiende a limitarse a la cavidad oral y la mandíbula, pero también puede afectar la piel, los ganglios linfáticos, la médula ósea, los pulmones y los intestinos. [17]. En el contexto posterior al trasplante, la piel y los ganglios linfáticos son los sitios más comunes de enfermedad. verdeling [18].
El PBL cutáneo primario es muy raro. Las características clínicas incluyen nódulos morados, erythemateus placas infiltradas y ulcerativas o infiltreren lesiones en las piernas [15,17].
El tratamiento para el PBL no se ha estandarizado. Las opciones de tratamiento incluyen:
- Chemotherapie
- chirurgische excisie
- Gecombineerde behandeling
- Terapia antirretroviral de gran actividad en el caso de PBL relacionados con el VIH.
El pronóstico de PBL es malo, con mediaan- supervivencia de 8 meses [16].