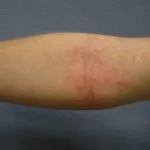
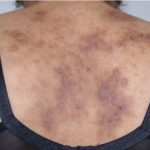
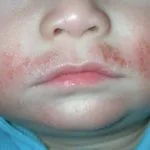
introduzione
Sono stati condotti tre studi clinici cardine di fase 3 per valutare dupilumab nel trattamento di atopica dermatite.
Dupilumab (Dupixent ™; Sanofi, Parigi, Francia; Regeneron, New York, USA) Ha mostrato risultati efficacia e un profilo di sicurezza favorevole in due studi cardine di fase 3 in monoterapia per la dermatite atopica da moderata a grave e in concomitante amministrazione con attuale corticosteroidi.
La Food and Drug Administration (FDA) statunitense ha concesso a dupilumab a designazione di terapia innovativa; La Biologics License Application (BLA) per dupilumab è stata recentemente accettata per la revisione prioritaria dalla FDA con una data di azione prevista per il 29 marzo 2017.
Dupilumab inibisce la segnalazione di interleuchina (IL) -4 e IL-13, due tasti citochine necessaria per la risposta immunitaria di tipo 2 (inclusa Th2), che si ritiene sia un fattore importante nella dermatite atopica.
Prova dell'efficacia di dupilumab dagli studi SOLO 1 e SOLO 2
- L'approvazione della FDA di dupilumab si baserà sui risultati di efficacia e sicurezza di tre studi di fase 3 (SOLO 1 & 2 e CHRONOS) nel programma mondiale LIBERTY per la dermatite atopica che ha arruolato più di 2.500 pazienti.
- Lo scopo degli studi era valutare dupilumab in monoterapia (SOLO 1 e SOLO 2) e in somministrazione concomitante con corticosteroidi topici (CHRONOS), in pazienti adulti con dermatite atopica da moderata a grave la cui malattia non è adeguatamente controllata con terapie topiche prescritte. .
- Gli studi SOLO 1 e SOLO 2 erano identici, multinazionali e doppio cieco e comprendevano rispettivamente 671 e 708 adulti con dermatite atopica per i quali erano stati somministrati farmaci topici controindicato o non ha fornito abbastanza controllo.
- I pazienti sono stati randomizzati in un rapporto 1: 1: 1 per ricevere, per 16 settimane, sottocutaneo dupilumab (300 mg) o placebo settimanalmente o la stessa dose di dupilumab ogni due settimane in alternanza con placebo.
- I pazienti avevano una malattia da moderata a grave, con a mediano 50% di superficie corporea (BSA) affetta da dermatite atopica e durata media della malattia di 25 anni.
- L'uso di agenti topici per la dermatite atopica non era consentito se non come terapia di salvataggio per i sintomi non controllati.
- PER base, i pazienti avevano un punteggio IGA (Investigator's Global Assessment) di 3 o superiore e a Eczema Area e indice di gravità (EASI) punteggio di 16 o più.
- il primario L'endpoint era un punteggio chiaro o quasi chiaro (0 o 1) sull'IGA (Investigator's Global Assessment) alla settimana 16, accompagnato da una riduzione di almeno 2 punti rispetto al basale. Un endpoint secondario chiave era un miglioramento di almeno 75% nell'area dell'eczema e nell'indice di gravità (EASI-75), considerato un endpoint co-primario dalle autorità di regolamentazione in Giappone e nell'Unione europea.
- In SOLO 1, l'outcome primario è stato raggiunto in 85 pazienti (38%) che hanno ricevuto dupilumab a settimane alterne e in 83 (37%) che hanno ricevuto dupilumab settimanalmente, rispetto a 23 (10%) che hanno ricevuto placebo (P <0,001 para ambas comparaciones con placebo).
- I risultati erano simili in SOLO 2, con l'outcome primario in 84 pazienti (36%) che ricevevano dupilumab a settimane alterne e 87 (36%) che ricevevano dupilumab settimanalmente, rispetto a 20 (8%) che ricevevano placebo (P <0,001 para ambas comparaciones).
- Inoltre, in entrambi gli studi è stato riportato un miglioramento dal basale alla settimana 16 di almeno 75% nell'area dell'eczema e nell'indice di gravità in un numero significativamente maggiore di pazienti che ricevevano ciascun regime di dupilumab rispetto ai pazienti che ricevevano placebo (P <0,001 para todas las comparaciones).
- La Tabella 1 fornisce un riepilogo dell'efficacia di dupilumab SOLO negli studi clinici 1 e 2.
Tabella 1. Miglioramenti nella dermatite atopica a 16 settimane
|
Placebo |
Dupilumab ogni 2 settimane |
Dupilumab settimanalmente |
P valore vs placebo |
|
|
IGA (SOLO 1) |
10% |
38% |
37% |
<0,0001 |
|
IGA (SOLO 2) |
9% |
36% |
36% |
<0,0001 |
|
EASI-75 (SOLO 1) |
15% |
51% |
53% |
<0,0001 |
|
EASI-75 (SOLO 2) |
12% |
44% |
48% |
<0,0001 |
- Dupilumab è stato anche associato a un miglioramento degli endpoint clinici secondari, inclusa una riduzione di prurito e sintomi di ansia o depressione e miglioramento della qualità della vita.
- La riduzione dell'intensità quotidiana del prurito riportata dal paziente, misurata dalla valutazione numerica del prurito Scala (NRS), era un endpoint secondario che è stato raggiunto a 2, 4 e 16 settimane.
- L'NRS per il prurito varia da 0 (nessun prurito) a 10 (peggior prurito immaginabile).
- A 16 settimane, SOLO 1 e SOLO 2, rispettivamente, il 41 e il 36 percento dei pazienti che ricevevano dupilumab 300 mg a settimane alterne e il 40 e il 39 percento dei pazienti che ricevevano dupilumab 300 mg settimanalmente, ottenuto una riduzione di quattro punti o più. sul punteggio NRS rispetto al 12 e al 10 percento con il placebo (P <0,001 para todos los regímenes y ensayos).
- I partecipanti hanno completato la scala HADS (Hospital Anxiety and Depression Scale) all'inizio dello studio ea 16 settimane.
- In totale HADS, i pazienti placebo hanno migliorato di 3,0 punti rispetto a 5,2 punti per entrambi i gruppi dupilumab in SOLO 1 (P = 0.0006 dupilumab due volte a settimana, P = 0,0003 dupilumab settimanalmente).
- SOLO 2, i pazienti trattati con placebo hanno migliorato di 0,8 punti rispetto a 5,1 e 5,8 punti nei gruppi dupilumab due volte alla settimana e alla settimana, rispettivamente (entrambi P <0,0001).
- Reazioni al sito di iniezione e congiuntivite erano più comuni nei gruppi dupilumab rispetto ai gruppi placebo.
- La linea di base mediana Dermatologia Il punteggio dell'indice di qualità della vita era 15 nelle due prove parallele. La percentuale collettiva di pazienti che hanno sperimentato un miglioramento di almeno 4 punti, che è considerata una risposta clinicamente significativa, è stata di 29,11 TP1T in controllo S, rispetto a 68,6% nei pazienti con dupilumab a settimane alterne e 60,2% con dupilumab settimanale.
- In conclusione, in due studi di fase 3 di design identico che hanno coinvolto pazienti con dermatite atopica, dupilumab ha migliorato i segni ei sintomi della dermatite atopica, inclusi prurito, sintomi di ansia e depressione e qualità della vita, rispetto con placebo. Sono necessari studi più lunghi per valutare l'efficacia e la sicurezza a lungo termine di dupilumab.
Reazioni avverse: esperienza in studi clinici
- Eventi avversi osservati in> 5% di pazienti che partecipano a studi clinici chiave su dupilumab sono riassunti nella tabella sottostante.
|
Evento |
SOLO 1 |
SOLO 2 |
||||
|
N. pazienti (%) |
Placebo qw (n = 222) |
Dupilumab 300 mg ogni 2 settimane (n = 229) |
Dupilumab 300 mg una volta al giorno (n = 218) |
Placebo qw (n = 234) |
Dupilumab 300 mg ogni 2 settimane (n = 236) |
Dupilumab 300 mg una volta al giorno (n = 237) |
|
Nasofaringite |
17 (8) |
22 (10) |
25 (12) |
22 (9) |
20 (9) |
20 (8) |
|
Congiuntivite |
2 (1) |
11 (5) |
7 (3) |
1 (<1) |
9 (4) |
9 (4) |
|
Tratto respiratorio superiore infezione |
5 (2) |
6 (3) |
11 (5) |
5 (2) |
7 (3) |
9 (4) |
|
Reazione al sito di iniezione |
13 (6) |
19 (8) |
41 (19) |
52 (16) |
32 (14) |
31 (13) |
|
Dermatite atopica esacerbazione |
67 (30) |
30 (13) |
21 (10) |
81 (35) |
32 (14) |
38 (16) |
|
Mal di testa |
13 (6) |
21 (9) |
11 (5) |
11 (5) |
19 (8) |
22 (9) |
|
Congiuntivite allergica |
2 (1) |
12 (5) |
7 (3) |
2 (1) |
2 (1) |
3 (1) |
Follow-up a lungo termine: evidenze dagli studi clinici CHRONOS
- Dupilumab utilizzato con corticosteroidi topici (TCS) era più alto al solo trattamento TCS in uno studio di fase 3 a lungo termine (1 anno) (LIBERTY AD CHRONOS) in pazienti con dermatite atopica da moderata a grave non adeguatamente controllata.
- Un totale di 740 pazienti adulti con dermatite atopica da moderata a grave sono stati arruolati in CHRONOS.
- Tutti i pazienti non erano adeguatamente controllati con farmaci topici e sono stati valutati utilizzando la scala di valutazione globale dello sperimentatore (IGA) di 5 punti, che varia da 0 (chiaro) a 4 (grave); I criteri di ingresso richiedevano un punteggio iniziale di 3 o 4.
- I pazienti sono stati valutati anche utilizzando l'Eczema Area and Severity Index (EASI) e altre misure.
- Tutti i pazienti hanno iniziato il trattamento quotidiano con un TCS di media potenza o un TCS a bassa potenza nelle aree del corpo in cui il TCS di media potenza è considerato non sicuro.
- I pazienti erano randomizzato 3: 1: 3 nei seguenti gruppi di trattamento (tutti in combinazione con TCS): dupilumab 300 mg per via sottocutanea una volta alla settimana (n = 319), dupilumab 300 mg per via sottocutanea ogni due settimane (n = 106) o placebo (n = 315).
- Questo disegno ha consentito una potenza sufficiente per gli endpoint di efficacia in entrambi i gruppi di dupilumab, aumentando al contempo i dati di sicurezza disponibili sul regime di dosaggio più comune.
I risultati dell'endpoint co-primario alla settimana 16 erano:
- Il 39% dei pazienti che hanno ricevuto dupilumab 300 mg a settimana con TCS o dupilumab 300 mg a settimane alterne con TCS è riuscito a pulire o quasi pulire la pelle lesioni (IGA 0 o 1), rispetto al 12% dei pazienti che hanno ricevuto placebo con TCS (P <0,0001).
- Il 64% dei pazienti che hanno ricevuto dupilumab 300 mg settimanalmente con TCS e il 69% dei pazienti che hanno ricevuto dupilumab 300 mg ogni due settimane con TCS hanno ottenuto l'EASI-75, una riduzione del 75% in un indice che misura la gravità dell'eczema, rispetto al 23 per cento dei pazienti. ricevere placebo con TCS (P <0,0001).
I risultati dell'endpoint co-primario alla settimana 52 erano:
- Il 40% dei pazienti che hanno ricevuto dupilumab 300 mg a settimana con TCS e il 36% dei pazienti che hanno ricevuto dupilumab 300 mg ogni due settimane con TCS ha ottenuto l'eliminazione o quasi l'eliminazione delle lesioni cutanee (IGA 0 o 1 ), rispetto al 12,5% dei pazienti. ricevere placebo con TCS (P <0,0001).
- Il 64% dei pazienti che hanno ricevuto 300 mg a settimana con TCS e il 65% dei pazienti che hanno ricevuto 300 mg ogni due settimane con TCS hanno raggiunto l'EASI-75, rispetto al 22% con placebo con TCS (P <0,0001).
- Il tasso complessivo di eventi avversi è stato paragonabile tra il gruppo dupilumab con TCS (83% per il gruppo di dosaggio settimanale (qw) e 88% per il gruppo di dosaggio ogni due settimane (q2w)) e il gruppo placebo con TCS ( 84%).
- Gli eventi avversi osservati per avere un tasso più elevato con dupilumab includevano reazioni nel sito di iniezione (20 (qw) e 16% (q2w) per dupilumab; 9% per placebo) e congiuntivite (19 (qw) e 13 (q2w). ) per cento dupilumab; 8% placebo); Il 22% dei pazienti che hanno ricevuto placebo e 23 (qw) e 28% (q2w) dei pazienti che hanno ricevuto dupilumab hanno riportato una storia di congiuntivite allergica all'ingresso nello studio.
Passaggi successivi con dupilumab
- Dupilumab è un innovativo farmaco sperimentale di prima classe che ha dimostrato un'efficacia significativa e un profilo di sicurezza favorevole in due studi cardine di fase 3 in monoterapia per la dermatite atopica da moderata a grave (SOLO 1 e SOLO 2) e nella somministrazione concomitante con corticosteroidi topici (CHRONOS).
- Ci sono stati miglioramenti clinicamente significativi e significativi nella pulizia della pelle (punteggi IGA), gravità della malattia (punteggi EASI), sintomi (prurito NRS) e qualità della vita correlata alla salute.
- Le tossicità identificate erano gestibili e reversibili con l'interruzione del trattamento.
- Studi e studi più lunghi che includono solo pazienti con malattia grave e che non sono idonei sistemico Gli immunosoppressori sono necessari per valutare ulteriormente l'efficacia e la sicurezza di dupilumab.
- Secondo il produttore, Regeneron, gli studi cardine di fase 3 di dupilumab in pediatrico La dermatite atopica nei bambini dai 6 mesi ai 17 anni inizierà nel 2017.