Cos'è cobimetinib?
Cobimetinib (Cotellic™, Genentech Inc. California, USA) è un farmaco da prescrizione utilizzato, in combinazione con vemurafenib, per il trattamento di pazienti con melanoma.
Cobimetinib ha ricevuto l'approvazione della Food and Drug Administration (FDA) statunitense negli Stati Uniti nel 2015. Nell'aprile 2017, Medsafe ha approvato cobimetinib per il trattamento dei pazienti con melanoma in Nuova Zelanda.
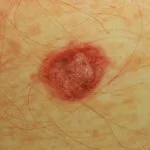
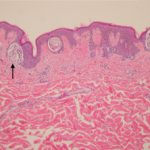
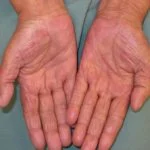
Melanoma metastatico
Melanoma metastatico
Melanoma metastatico
Melanoma metastatico
Chi dovrebbe assumere cobimetinib?
Cobimetinib, in associazione con vemurafenib, è indicato per il trattamento di pazienti con non resecabile o metastatico melanoma, in cui il Cancro che si è diffuso ad altre parti del corpo o non può essere rimosso chirurgicamente. Un indicatore di questo melanoma è un'anomalia gene Ha chiamato il BRAF V600E o V600K mutazione, che deve essere confermato in tumore campioni prima di iniziare il trattamento.
Cobimetinib non è indicato per il trattamento di pazienti di tipo normale o selvaggio. BRAF gene.
Come funziona cobimetinib?
Cobimetinib è un piccolo molecola inibitore che blocca il MEK enzima, un componente della cascata delle chinasi nel mitogeno attivato proteina chinasiMAPK) percorso. I componenti delle vie MAPK sono frequentemente mutati nei pazienti con il malvagio melanoma, in particolare RAF isoforma BRAF. Mutazioni di BRAF causare un'attivazione costitutiva di queste vie di segnalazione, che possono portare al cancro.
Cobimetinib e vemurafenib prendono di mira due diverse chinasi nella via MAPK. Studi clinici hanno dimostrato che la combinazione di cobimetinib con vemurafenib migliora la sopravvivenza nei pazienti con melanoma che ospitano il BRAF Mutazione V600.
Come viene somministrato cobimetinib?
Dose consigliata
Cobimetinib è disponibile in compresse da 20 mg con il marchio Cotellic.
- La dose raccomandata è di 60 mg una volta al giorno per i primi 21 giorni di ogni ciclo di 28 giorni, continuata fino a progressione della malattia o intollerabile. tossicità accade.
- Cobimetinib può essere assunto con o senza cibo.
- Se si dimentica una dose o si verifica vomito durante l'assunzione della dose, riprendere la somministrazione con la dose successiva programmata.
Vemurafenib (ZELBORAF™) deve essere assunto ogni 12 ore ogni giorno del ciclo di 28 giorni (nessun periodo di riposo). Se dimentica una dose di vemurafenib, dovrebbe prenderla non appena se ne ricorda. Non recuperi la dose dimenticata se la dose dimenticata è entro 4 ore dalla successiva dose programmata.
Uso di cobimetinib in popolazioni specifiche
Gestante
I dati sull'uso di cobimetinib nelle donne in gravidanza non sono disponibili per informare di un rischio associato al farmaco di gravi difetti alla nascita e aborto spontaneo. Sulla base dei risultati degli studi sulla riproduzione animale e del suo meccanismo d'azione, cobimetinib può causare danni al feto. Le donne in gravidanza dovrebbero essere avvertite del potenziale rischio per il feto.
Donne che allattano
Non ci sono informazioni sulla presenza di cobimetinib nel latte materno o sui suoi effetti su un lattante. Quando si prescrive cobimetinib alla madre, deve essere considerato il potenziale rischio-beneficio. Le donne che allattano devono essere avvisate di non allattare durante il trattamento con cobimetinib e per 2 settimane dopo la dose finale.
Bambini
La sicurezza e l'efficacia di cobimetinib nei bambini non sono state valutate.
Femmine e maschi in età riproduttiva
Le pazienti in età fertile devono essere informate di usare un metodo contraccettivo efficace durante il trattamento con cobimetinib e per 2 settimane dopo la dose finale. Sulla base dei risultati negli animali, cobimetinib può ridurre la fertilità nelle femmine e nei maschi con potenziale riproduttivo.
Anziani
Gli studi clinici con cobimetinib non hanno incluso un numero sufficiente di persone di età pari o superiore a 65 anni per determinare se rispondono in modo diverso rispetto ai soggetti più giovani.
Individui con epatica o renale disabilità
Non è necessario alcun aggiustamento della dose di cobimetinib nei pazienti con compromissione epatica lieve (punteggio Child-Pugh A), moderata (Child-Pugh B) o grave (Child-Pugh C). non dedicato farmacocinetica Uno studio è stato condotto in pazienti con insufficienza renale. L'aggiustamento della dose non è raccomandato per l'insufficienza renale da lieve a moderata (clearance della creatinina da 30 a 89 ml/minuto) sulla base dei risultati dell'analisi farmacocinetica di popolazione. Non è stata stabilita una dose raccomandata per i pazienti con grave insufficienza renale.
Quali sono i possibili effetti collaterali di cobimetinib?
Gli effetti collaterali comuni includono:
- Diarrea
- Eruzione
- Fotosensibilità
- Nausea
- Stomatite
- Febbre
- Alopecia
- Trombocitopenia.
Gli effetti collaterali rari ma potenzialmente gravi includono:
- Grave diarrea che porta a disidratazione e insufficienza renale.
- Rabdomiolisi
- tossicità cardiaca
- Distacco della retina
- Tossicità embrionale e fetale
- Dolori articolari (artralgia).
Epatotossicità
elevazioni in siero aminotransferasi e alcalina fosfatasi I livelli sono comuni durante la terapia con vemurafenib e sono ancora più comuni se combinati con cobimetinib.
Casi di danno epatico clinicamente evidente con ittero Sono stati segnalati durante gli studi clinici sulla terapia con cobimetinib e vemurafenib, ma le caratteristiche cliniche, il decorso e gli esiti di questi episodi non sono stati descritti in dettaglio.
Il percorso MAPK inibitori come classe a cui sono spesso associati transitorio aumenti degli enzimi sierici e, più raramente, con casi di danno epatico clinicamente evidente, ma le caratteristiche cliniche non sono state descritte e l'associazione con cobimetinib non è stata chiaramente definita.
Il tasso di danno epatico clinicamente significativo e insufficienza epatica associati agli inibitori della protein chinasi è aumentato nei pazienti con cirrosi o insufficienza epatica a causa del carico di tumore al fegato. L'etichetta del prodotto cobimetinib raccomanda il monitoraggio di routine dei test di funzionalità epatica durante il trattamento.
Aumenti dell'aminotransferasi sierica superiori a cinque volte il limite superiore della norma (se confermati) dovrebbero portare a una sospensione temporanea, che dovrebbe diventare permanente se questi valori di laboratorio non migliorano in modo significativo o si risolvono entro poche settimane.
Non sembra esserci alcuna reattività crociata con altri tirosina chinasi ricevitore inibitori. In alcune situazioni, può essere appropriato passare a un altro inibitore della protein chinasi.
Rischio di nuovi tumori
Cobimetinib in combinazione con vemurafenib può causare nuovi tumori della pelle. Questi possono includere:
- Cutaneo squamoso cellula carcinoma
- Cheratoacantoma
- Basale carcinoma cellulare.
Problemi di cuore
Cardiomiopatia, definito sintomatico e asintomatico ridotta espulsione dal ventricolo sinistro frazione (LVEF), può verificarsi con cobimetinib.
La sicurezza di cobimetinib non è stata stabilita nei pazienti con base LVEF inferiore al limite istituzionale inferiore della norma o inferiore a 50%.
La LVEF deve essere valutata prima dell'inizio di cobimetinib, 1 mese dopo l'inizio e successivamente ogni 3 mesi fino alla sospensione del farmaco. Eventi ventricolari sinistri disfunzione deve essere gestito interrompendo, riducendo o interrompendo il trattamento.
Interazioni farmacologiche
Cobimetinib è metabolizzato nel fegato attraverso il sistema del citocromo P450, prevalentemente CYP3A, ed è suscettibile alle interazioni farmacologiche con potenti inibitori o induttori di questo enzima microsomiale.
La co-somministrazione di cobimetinib con itraconazolo (un potente inibitore del CYP3A4) ha aumentato cobimetinib sistemico esposizione di 6,7 volte.
Concorrente L'uso di cobimetinib e inibitori forti o moderati del CYP3A deve essere evitato. Se l'uso simultaneo a breve termine (14 giorni o meno) di inibitori moderati del CYP3A, inclusi alcuni antibiotici (p. es., eritromicina, ciprofloxacina) è inevitabile (14 giorni o meno), la dose di cobimetinib deve essere ridotta da 60 a 20 mg
Un'alternativa a un inibitore del CYP3A forte o moderato deve essere utilizzata nei pazienti che assumono una dose ridotta di cobimetinib (40 o 20 mg al giorno). Dopo l'interruzione di un inibitore moderato del CYP3A, cobimetinib deve essere ripreso alla dose precedente.
La co-somministrazione di cobimetinib con un potente induttore del CYP3A può ridurre l'esposizione sistemica di cobimetinib di oltre 80% e ridurne efficacia. Deve essere evitato l'uso concomitante di cobimetinib e induttori forti o moderati del CYP3A, inclusi ma non limitati a carbamazepina, efavirenz, fenitoina, rifampicina ed erba di San Giovanni.
Controindicazioni
Cobimetinib deve essere interrotto nelle seguenti circostanze:
- Storia di problemi di salute mentale, inclusi pensieri suicidi, depressione, ansia o problemi di umore.
- Concorrente infezione che non va via o continua a tornare
- Tubercolosi (TB) o stretto contatto con qualcuno con la tubercolosi
- Ricevuto di recente o programmato per ricevere un vaccino
- Stai pianificando una gravidanza
- Allattamento al seno o pianificazione di allattare.