Wat is angioimmunoblastisch? T-cel lymfoom?
Angioimmunoblastisch T-cellymfoom is zeldzaam nodaal perifere T-cellymfoom (PTCL) dat veroorzaakt systemisch symptomen en ernstige immuundeficiëntie [1]. Soms veroorzaakt het een uitslag.
Angioimmunoblastisch T-cellymfoom wordt gekarakteriseerd histologisch voor polymorf infiltreren voornamelijk betrekken lymfe knooppunten, a proliferatie Hoog endotheel venulenY folliculair dendritische cellen [2].
Wie krijgt angioimmunoblastisch T-cellymfoom?
Angioimmunoblastisch T-cellymfoom is zeldzaam.
- perifere T-cel lymfomen omvatten van 10 tot 15% van allemaal lymfoïde maligniteiten [1,3]
- Angioimmunoblastisch T-cellymfoom is verantwoordelijk voor 15 tot 20% van perifere T-cellymfomen en 1 tot 2% van non-Hodgkin-lymfomen [2,4].
Angioimmunoblastisch T-cellymfoom treft meestal oudere volwassenen [4]. de mediaan- de leeftijd van diagnose is 62 tot 65 jaar. Incidentie het is hetzelfde bij mannen en vrouwen [4].
Er zijn geen risicofactoren voor angioimmunoblastisch T-cellymfoom vastgesteld.
Wat veroorzaakt angioimmunoblastisch T-cellymfoom?
De oorsprongscel van angioimmunoblastisch T-cellymfoom is de folliculaire helper-T-cel. [4]. Kwaadaardige De transformatie is in verband gebracht met mutaties in de epigenetisch regelgeversTET2, HDI2 Y DNMT3A), de homoloog van Ras gen lid van gezin Arhoa) en T-cellen ontvanger traject (CD28, FYN, PLCG1, KAART11, Q13K artikelen, CTNNB1Y GTF2I) [4].
Angioimmunoblastisch T-cellymfoom wordt bevorderd door overexpressie van angiogeen bemiddelaars (factoren die de ontwikkelen van aderen), Wat vasculair endotheel groeifactor (VEGF) en interleukine (IL)-8, en cytokinen Wat zijn ze pro-inflammatoir (IL6, IL18), immunosuppressief (IL10), of proliferatie induceren (IL21) [4,5].
Infectieziekten geassocieerd met angioimmunoblastisch T-cellymfoom omvatten het Epstein-Barr-virus (EBV, de oorzaak van infectieuze mononucleosis), humaan herpesvirus 6 (HHV-6) (de oorzaak van roseola), HHV-8 (de oorzaak van Kaposi sarcoom), humaan immunodeficiëntievirus (hiv), bacterieel infecties en schimmelinfecties [4].
De rol van het Epstein Barr-virus
EBV sets voor het leven aanhoudend infectie in B-cellen. Immunodeficiëntie veroorzaakt door angioimmunoblastisch T-cellymfoom reactiveert EBV [4,6–8].
- EBV-geïnfecteerde B-cellen zijn aanwezig in 58 tot 97% van patiënten met angioimmunoblastisch T-cellymfoom [8,9].
- EBV (en mogelijk HHV-6) kan een rol spelen bij het bevorderen van ziekteprogressie door middel van cytokinemodulatie. chemokinenen membraanreceptoren [6].
- Van EBV wordt gedacht dat het de levensduur van B-cellen verlengt en kan veroorzaken genetisch afwijkingen, zoals het voorkomen van c-myc-geïnduceerde apoptose, leidend tot B-cellymfoom [4,8,10]. Zie geassocieerd met het Epstein-Barr-virus lymfoproliferatief stoornissen.
Wat zijn de klinische kenmerken van angioimmunoblastisch T-cellymfoom?
Meer dan 70% van de patiënten met angioimmunoblastisch T-cellymfoom vertoont constitutionele symptomen. Deze omvatten koorts, koude rillingen, nachtelijk zweten, ongemak, gewichtsverlies, artralgieen in 50% uitslag [11].
lymfadenopathie Y hepatosplenomegalie zijn meestal aanwezig bij het examen. Meervoud ontboezemingen, ascites, neurologisch Gastro-intestinale tekenen en symptomen komen minder vaak voor [4].
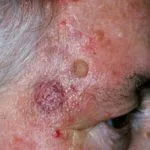
huid kenmerken van angioimmunoblastisch T-cellymfoom
Angioimmunoblastisch T-cellymfoom presenteert zich meestal met een niet-specifieke huiduitslag [11]. Het kan er ook toe leiden papels, knobbeltjes, platen, zweren, petechiënen zelden erytrodermie [8,11,12].
Uitslag geassocieerd met angioimmunoblastisch T-cellymfoom
De patiënt had een EBV-geassocieerd T-cellymfoom
Wat zijn de complicaties van angioimmunoblastisch T-cellymfoom?
Vooral patiënten met angioimmunoblastisch T-cellymfoom lopen een verhoogd risico op secundair B-cellymfoom diffuus grootcellig B-cellymfoom (DLBCL) en, minder vaak, Hodgkin-lymfoom of plasmacytoom [13].
Er zijn 30 gedocumenteerde gevallen van EBV-geassocieerde B-cellymfomen bij patiënten met angioimmunoblastisch T-cellymfoom (november 2019) [14-16].
EBV-geïnduceerd diffuus grootcellig B-cellymfoom kan zich ook presenteren met bevindingen op de huid, zoals zwerende papels, knobbeltjes en abcessen [16].
Hoe wordt de diagnose angioimmunoblastisch T-cellymfoom gesteld?
Laboratorium afwijkingen erbij betrekken:
- Bloedarmoede (vaak hemolytisch, met een positieve Coombs-test)
- eosinofilie
- Polyklonale hypergammaglobulinemie
- antinucleair antistoffen (ANA)
- Koud agglutininen
- cryoglobulinemie
- circulerende immuuncomplexen
- Hoog serum lactaatdehydrogenase (LDH) en bèta-2-microglobuline
- hoge EBV.
Perifeer bloed leukocytose met lymfocytose komt niet vaak voor. Flowcytometrie kan worden gebruikt om te detecteren afwijkend T-cellen [17].
De diagnose angioimmunoblastisch T-cellymfoom wordt meestal gesteld door lymfeklier biopsie.
Er zijn vijf angioimmunoblastische T-cellymfomen histopathologisch patronen op de huid.
- een ondiep perivasculair infiltraat samengesteld uit eosinofielen Y lymfocyten dat gebrek atypie (het meest voorkomende patroon)
- Een karig perivasculair infiltraat met atypisch lymfocyten
- Een dicht oppervlakkig en diep infiltraat van pleomorf lymfocyten
- vasculitis, met of zonder atypische lymfocyten
- necrotiserend granulomen.
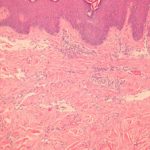
Histologie van angioimmunoblastisch T-cellymfoom
H&E x 20
H&E x 40
H&E x 400
Het immunofenotype van neoplastisch komt meestal overeen met folliculaire T-helpercellen (CD3+, CD4+, CD8-, CD10+, PD-1+, ICOS+, bcl-6+, chemokine ligand CXCL13+) meer groepen van CD21+ folliculaire dendritische cellen.
EBV-positief gevonden in a immunohistochemie de plek is hoger in de meer volwassen verwondingen en vormt af en toe vage patronen [18].
Immunohistochemie van angioimmunoblastisch T-cellymfoom
Anti-CD3 x 20
Anti-cd 20 x 20
Anti-cd 21 x 20
Anti-Epstein vat x 200
Anti-PD1 x 100
Welke is de differentiële diagnose voor cutaan angioimmunoblastisch T-cellymfoom?
De differentiële diagnose van cutaan angio-immunoblastisch T-cellymfoom hangt af van de morfologie van de uitslag, maar kan omvatten:
- drugs uitslag
- virale exantheem
- Atypische mycobacteriële infectie of andere opportunistische infectie
- Andere oorzaken van erytrodermie.
Wat is de behandeling van angioimmunoblastisch T-cellymfoom?
Vanwege de zeldzaamheid van angioimmunoblastisch T-cellymfoom wordt de behandeling over het algemeen geleid door prospectieve fase II-onderzoeken [4].
- El tratamiento más común es a base de antraciclina. chemotherapie como CHOP (ciclofosfamida, doxorrubicina, vincristina y prednisona / prednisolona).
- Consolidación de seguimiento con células madre autólogas transplantatie ha mostrado resultados prometedores [19].
- Ensayos de histona desacetilasa (HDAC) remmers, agentes hipometilantes y anticuerpos anti-CD30 están en curso [20–23].
¿Cuál es el resultado del linfoma angioinmunoblástico de células T?
El linfoma angioinmunoblástico de células T suele ser agresivo con una mediana de supervivencia de menos de 3 años, incluso con tratamiento intensivo. Los pacientes suelen presentarse con enfermedad en estadio III-IV tardío, y las tasas de supervivencia se han citado como 33% a los 5 años y 29% a los 7 años [18].
- La quimioterapia CHOP estándar tiene una tasa de respuesta general del 70% al 80% y una supervivencia libre de progresión a 5 años del 10% al 20% [8,24].
- El BEAM de seguimiento (carmustina, etopósido, citarabina, melfalán) y el trasplante autólogo de células madre tienen una tasa de supervivencia libre de progresión a 5 años de alrededor del 40% [25].
EBV circulante DNA se pueden controlar los niveles; los niveles más altos se asocian con más pobres voorspelling. Sin embargo, la presencia de EBV en los tumores ganglionares no altera el pronóstico.
Los linfomas secundarios de células B tienen un pronóstico típicamente desfavorable. Ocho de cada 30 pacientes con linfoma de células B asociado al VEB sobrevivieron más de 12 meses [14–16].