Invoering
In februari 2017 kreeg de biologische behandeling brodalumab (Siliq™; Valeant Pharmaceuticals, NJ, VS) goedkeuring van de Amerikaanse Food and Drug Administration (FDA) voor de behandeling van psoriasis bij volwassen patiënten die niet reageerden op andere behandelingen.
Valeant verwacht in de tweede helft van 2017 te beginnen met het op de markt brengen en commercialiseren van brodalumab in de Verenigde Staten.
Vanwege het waargenomen risico op zelfmoordgedachten en -gedrag, bevat de etikettering van brodalumab een waarschuwing in een kader en is het medicijn alleen verkrijgbaar via een beperkt programma onder het FDA's Risk Evaluation and Mitigation Strategies (REMS)-programma. Hieronder staan opmerkelijke programma-eisen.
- Voorschrijvers moeten gecertificeerd zijn met het REMS-programma en patiënten adviseren over het risico op zelfmoordgedachten en -gedrag.
- Patiënten met nieuwe of verslechterende symptomen van depressie of suïcidaliteit moeten, indien van toepassing, worden doorverwezen naar een beroepsbeoefenaar in de geestelijke gezondheidszorg.
- patiënten zouden moeten teken een patiënt-voorschrijver overeenkomstformulier en wees bewust van de noodzaak om medische hulp te zoeken als ze nieuwe of verergerende zelfmoordgedachten of -gedrag, gevoelens van depressie, angst of andere stemmingswisselingen ervaren.
- Apotheken moeten ook gecertificeerd zijn met het REMS-programma en mogen brodalumab alleen verstrekken aan patiënten die bevoegd zijn om het medicijn te krijgen.
Een oorzakelijk verband tussen behandeling met brodalumab en een verhoogd risico op zelfmoordgedachten en -gedrag is niet vastgesteld.
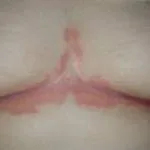
Chronische plaque psoriasis
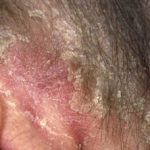
Hoofdhuid psoriasis
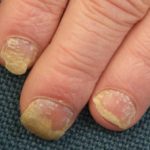
Handpsoriasis
Chronische plaque psoriasis
Waar wordt brodalumab voor gebruikt?
Brodalumab wordt gebruikt voor de behandeling van volwassen patiënten met matige tot ernstige ziekte. nummerplaat psoriasis die in aanmerking komen voor systemisch therapie of fototherapie en hebben gefaald of niet gereageerd op andere systemische therapieën.
Het wordt aanbevolen voor kandidaten voor wie systemische therapie of fototherapie geen resultaat of adequate behandeling heeft opgeleverd.
Hoe werkt brodalumab?
Brodalumab is een monoklonaal immunoglobuline G2 (IgG2) antilichaam dat remt opruiend reacties en bindt zich selectief aan de ontvanger van interleukine 17 (IL-17), op cytokine dat begint ontsteking.
De IL-17-receptor is een eiwit tot expressie gebracht op het celoppervlak en is een component van receptorcomplexen die door meerdere IL-17-families worden gebruikt cytokinenzoals IL-17A, IL-17F, IL-17C, IL-17A/F heterodimeer en IL-25. Blokkering van de IL-17-receptor remt door cytokine geïnduceerde reacties van IL-17, waaronder de afgifte van pro-inflammatoir cytokinen en chemokinen geassocieerd met pathogenese van psoriasis.
Hoe wordt brodalumab toegediend?
Brodalumab wordt toegediend subcutaan. Elke voorgevulde spuit (1,5 ml) bevat 210 mg brodalumab en is uitsluitend voor eenmalig gebruik.
- De aanbevolen dosis brodalumab is 210 mg toegediend per onderhuids injectie in week 0, 1 en 2, gevolgd door 210 mg om de 2 weken.
- Als na 12 tot 16 weken behandeling geen adequate respons is bereikt, moet de behandeling met brodalumab worden gestaakt.
- Brodalumab mag niet worden geïnjecteerd in gebieden waar de huid gevoelig, gekneusd, rood, hard, dik, geschubd, of aangetast door psoriasis.
- Brodalumab wel gecontra-indiceerd bij patiënten met de ziekte van Crohn omdat het geneesmiddel de ziekte kan verergeren.
- Patiënten met een voorgeschiedenis van latent Tuberculose moet worden behandeld vóór toediening van brodalumab, dat latente tuberculose kan reactiveren. infectie.
Het gebruik van brodalumab in specifieke populaties
Zwangere vrouw
Er zijn geen gegevens beschikbaar over het gebruik van brodalumab bij zwangere vrouwen om clinici te informeren over het geneesmiddelgerelateerde risico op ernstige geboorteafwijkingen en miskraam.
niet nadelig ontwikkelingsgericht Effecten bij drachtige apen zijn waargenomen na subcutane toediening van brodalumab tot 26 keer de maximaal aanbevolen dosis voor de mens. (Zie Veiligheid van medicijnen die tijdens de zwangerschap worden ingenomen voor meer informatie.)
Vrouwen die borstvoeding geven
Er is geen informatie over de aanwezigheid van brodalumab in moedermelk of de effecten ervan op de zuigeling. Bij het voorschrijven van brodalumab aan een zogende moeder moeten de mogelijke risico's en voordelen worden afgewogen. (Zie Borstvoeding en de huid).
Kinderen
De veiligheid en werkzaamheid van brodalumab zijn niet onderzocht in pediatrisch patiënten.
Oude mensen
Klinische onderzoeken met brodalumab omvatten onvoldoende proefpersonen van 65 jaar of ouder om te bepalen of oudere mensen anders zullen reageren dan jongere mensen.
Personen met lever of nier onbekwaamheid
Er zijn geen onderzoeken uitgevoerd om het gebruik van brodalumab bij patiënten met een lever- of nierfunctiestoornis te evalueren.
Wat zijn de risico's van brodalumab?
Bijwerkingen
De meest voorkomende Bijwerkingen (≥ 1% van patiënten) gemeld met brodalumab omvatten:
- Artralgie (gewrichtspijn)
- Hoofdpijn
- Vermoeidheid
- Diarree
- orofaryngeaal pijn (keelpijn)
- Misselijkheid
- Spierpijn (Spierpijn)
- Reacties op de injectieplaats
- Influenza
- Neutropenie (laag aantal witte bloedcellen)
- Paddestoelen infecties (zoals ringworm).
De volgende ernstige bijwerkingen zijn gemeld in klinische onderzoeken bij patiënten die werden behandeld met brodalumab:
- Zelfmoordgedachten en -gedrag
- Ernstige infecties zoals cryptokokken meningitis
- Latente reactivering van tuberculose
- verergering van de ziekte van Crohn.
Geneesmiddelinteracties
Er zijn geen gegevens beschikbaar over het vermogen van levende of geïnactiveerde vaccins om een immuunrespons op te wekken bij patiënten die met brodalumab worden behandeld. Levende vaccins mogen niet worden gebruikt tijdens de behandeling met brodalumab.
Het effect van geneesmiddelen die worden gemetaboliseerd door hepatisch cytochroom P450 enzymen (zoals warfarine en ciclosporine) kunnen tijdens de behandeling worden gewijzigd gelijktijdig toediening met brodalumab. Aanpassing van de doses van deze geneesmiddelen moet worden overwogen.
Contra-indicaties
Brodalumab is gecontra-indiceerd bij mensen die:
- U heeft een voorgeschiedenis van psychische problemen, waaronder zelfmoordgedachten, depressie, angst of stemmingsproblemen.
- Heb terugkerende infecties
- U heeft tuberculose of bent in nauw contact geweest met iemand met tuberculose.
- U heeft onlangs een vaccinatie gekregen of bent van plan deze te krijgen.
- van plan om zwanger te worden
- U geeft momenteel borstvoeding of bent van plan borstvoeding te geven.
Wat zijn de vooruitzichten voor behandeling met brodalumab?
Brodalumab heeft een acceptabel veiligheidsprofiel laten zien en is goed effectiviteit bij de behandeling van matige tot ernstige plaque psoriasis. Het biedt een belangrijke nieuwe therapie bij de behandeling van psoriasis waar er nog steeds een aanzienlijke onvervulde behoefte bestaat aan nieuwe middelen met nieuwe werkingsmechanismen, een snel intredend effect en een verbeterde en aanhoudende algehele huidklaring, terwijl het helpt om de therapietrouw van de patiënt te vergroten en de medicatie zo klein mogelijk te houden. specifieke veiligheidsproblemen.
Het huidige bewijs voor brodalumab is echter onvoldoende om het behoud van deze resultaten op de lange termijn te bevestigen.