Che cos'è ipogonadismo nelle femmine?
L'ipogonadismo nelle donne descrive la funzione inadeguata delle ovaie, con scarsa produzione di cellule germinali (ovuli) e sesso ormoniestrogeni e progesterone).
- Primario L'ipogonadismo si riferisce a una condizione delle ovaie (insufficienza ovarica primaria / ipogonadismo ipergonadotropo).
- L'ipogonadismo secondario si riferisce al fallimento del ipotalamo o ipofisi ghiandola (ipogonadismo ipogonadotropo).
Che cosa causa l'ipogonadismo nelle donne?
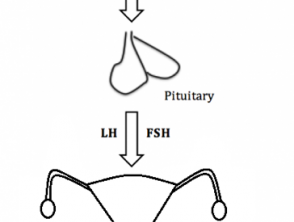
L'ipogonadismo nelle donne è dovuto all'interruzione di qualsiasi sezione del ipotalamico-Via asse ipofisario-ovarico (Figura 1). In un percorso dell'asse ipotalamo-ipofisi-ovaio correttamente funzionante:
- L'ipotalamo produce l'ormone di rilascio delle gonadotropine (GnRH) all'inizio della pubertà
- Il GnRH agisce quindi sulla ghiandola pituitaria, che produce follicoloormone stimolante (FSH) e ormone luteinizzante (LH)
- L'FSH e l'LH agiscono quindi sulle ovaie per stimolare la produzione di estrogeni e progesterone.
Figura 1. Percorso dell'asse ipotalamo-ipofisi-ovaio
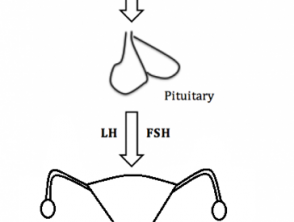
La via dell'asse ipotalamo-ipofisi-gonadi nelle donne
FSH, follicolo-stimolato; GnRH, gonadotropina - ormone di rilascio: LH, ormone luteinizzante.
Chi ha l'ipogonadismo?
L'insufficienza ovarica primaria e l'ipogonadismo secondario possono essere congenita o acquisito [1,2].
Insufficienza ovarica primaria congenita
Il meccanismo principale del deficit ovarico primario congenito rimane sconosciuto nella maggior parte dei casi. Alcuni casi sono legati a:
- Cromosomico anomalie, come Turner sindrome (45, X cariotipo), sindrome dell'X fragile e galattosemia (incapacità di elaborare lo zucchero galattosio)
- Disgenesia ovarica (organo anormale sviluppo) e agenesia (incapacità dell'organo a sviluppare durante lo sviluppo embrionale)
- Surrenale congenito iperplasia (Deficit di 17α-idrossilasi).
Insufficienza ovarica primaria acquisita
Le cause dell'insufficienza ovarica primaria acquisita includono:
- Farmaci, come clorambucile, ciclofosfamide e agenti alchilanti
- Radioterapia
- Autoimmune malattie inclusa la sindrome poliglandulare autoimmune di tipo 1
- Virale infezioni, comprese ooforite da parotite, tubercolosi (TB), malaria, varicella e
- Batterica infezioni, come Shigella
- Iatrogena malattia, come problemi dopo ovariectomia (rimozione chirurgica delle ovaie).
Ipogonadismo secondario congenito
L'ipogonadismo secondario congenito è un deficit di gonadotropine dovuto a a genetico mutazione, come nella sindrome di Kallmann.
Ipogonadismo secondario acquisito
L'ipogonadismo secondario acquisito può essere dovuto a un danno all'ipofisi / ipotalamo. Le cause dell'ipogonadismo secondario acquisito possono includere:
- Intracranica Occupare lo spazio lesioni (p. es., tumori e cisti)
- Infiltrante malattia (p. es., sarcoidosi ed emocromatosi)
- Infezione (per esempio, meningite e TB)
- Ipofisi apoplessia (sanguinamento nella ghiandola pituitaria)
- Trauma.
Le gonadotropine possono essere soppresse da:
- Cronico malattia (ad esempio, diabete, anoressia, obesità e renale patologia)
- Esercizio fisico eccessivo
- Malattia critica
- Oppiacei cronici, glucocorticoidio uso di steroidi anabolizzanti
- Iperprolattinemia (eccesso di prolattina, ormone che induce il latte).
Quali sono le caratteristiche cliniche dell'ipogonadismo nelle donne?
Le caratteristiche cliniche dell'ipogonadismo dipendono dall'età di presentazione. [3].
Carenza di estrogeni prima della pubertà
I sintomi di bassi livelli di estrogeni sono raramente presenti nell'ipogonadismo prima della pubertà. Le caratteristiche che si presentano sono l'assenza di sviluppo puberale (crescita ridotta e assenza di pube capelli) e primaria amenorrea (assenza di menarca).
Carenza di estrogeni dopo la pubertà
Dopo il completamento della pubertà, le caratteristiche dell'ipogonadismo includono:
- Amenorrea secondaria (cessazione delle mestruazioni regolari per 3 mesi o la cessazione delle mestruazioni irregolari per 6 mesi)
- Sintomi climaterici (perimenopausa): palpitazioni, intolleranza al calore, vampate di calore, sudorazioni notturne, irritabilità, ansia, depressione, disturbi del sonno, perdita della libido, capelli ruvidi, vaginale secchezza e stanchezza
- Sterilità.
Quali sono le complicazioni della carenza di estrogeni?
I rischi a lungo termine di carenza di estrogeni includono un aumento del rischio di osteoporosi e malattie cardiovascolari. Il rischio è maggiore con la prima insorgenza. Al contrario, il rischio di seno Cancro può essere leggermente ridotto.
Quali cambiamenti della pelle possono essere causati dall'ipogonadismo nelle donne?
Gli estrogeni svolgono un ruolo chiave nel mantenimento della salute della pelle. L'estrogeno aiuta a mantenere lo spessore della pelle e collagene livelli, elasticità e idratazione della pelle. Si ritiene inoltre che abbia un ruolo nella guarigione delle ferite. [4].
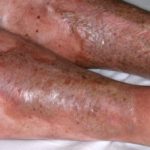
Bassi livelli di estrogeni sono associati a:
- Pelle secca e sottile
- Potenzialmente aumento delle rughe
- Guarigione ritardata della ferita
- Perdita di elasticità, spessore e umidità della pelle vulvare, con conseguente genito-urinario malessere.
I cambiamenti della pelle possono anche riflettere la causa sottostante dell'ipogonadismo; per esempio, iperpigmentazione Forse un cartello di una malattia autoimmune.
Come viene diagnosticato l'ipogonadismo?
Se si sospetta ipogonadismo dopo un'anamnesi e un esame dettagliati, si può seguire la seguente via di indagine.
- Il paziente deve essere indirizzato a uno specialista.
- Le indagini iniziali dovrebbero includere [5,6]:
- La gonadotropina corionica umana (hCG) esclude la gravidanza
- FSH e LH
- Estradiolo
- Ormone stimolante la tiroide (TSH): i disturbi della tiroide possono presentarsi con amenorrea
- Siero prolattina
- Pelvico ecografia esplorazione - prepuberanza.
interpretazione dei risultati
- Un test hCG positivo è dovuto alla gravidanza.
- Se lui utero è assente o sono presenti altre anomalie anatomiche, eseguire un test del cariotipo.
- Livelli bassi o bassi / normali di FSH e LH possono indicare ipogonadismo ipogonadotropo. UN Risonanza magnetica il cervello dovrebbe essere considerato.
- La prepuberanza, i livelli elevati di FSH e LH possono indicare un'insufficienza ovarica primaria. Gli ormoni surrenali devono essere valutati e deve essere eseguito un test del cariotipo.
- Un risultato elevato di prolattina dovrebbe sollecitare la considerazione di una risonanza magnetica ipofisaria.
Qual è il trattamento per l'ipogonadismo nelle donne?
Il trattamento dell'ipogonadismo è diretto a patologia quando possibile, aiutare la donna a diventare fertile se lo si desidera e prevenire le complicanze a lungo termine dell'ipoestrogenismo (cioè osteoporosi, aumento delle malattie cardiovascolari e urogenitale atrofia).
Come regola generale, le donne in età riproduttiva con ipoestrogenismo dovrebbero ricevere una terapia ormonale sostitutiva. Si dovrebbe chiedere il parere di uno specialista, in quanto vi sono potenziali complicazioni maggiori della terapia ormonale, come:
- Iperplasia endometriale e carcinoma nella terapia estrogenica incontrastata - è comune aggiungere a progestinico per fermare questo
- Aumento del rischio di cancro al seno, venoso tromboembolia, ictus e ischemico cardiopatia.
La terapia ormonale sostitutiva in postmenopausa è indicata per sintomi significativi.