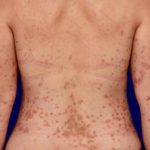
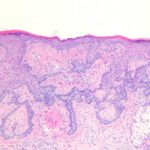
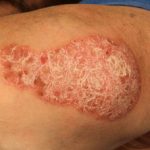
Introducción
El 26 de agosto de 2013, la Administración de Drogas y Alimentos de los EE. UU. (FDA) aprobó la brimonidina (Mirvaso®) actual gel, 0,33% * (Galderma Laboratories, Texas, EE. UU.) Para el tratamiento tópico de persistente (no-transitorio) facial eritema (enrojecimiento) de la rosácea en adultos de 18 años o mayores.
Es el primer y único tratamiento tópico aprobado por la FDA desarrollado e indicado específicamente para el eritema facial persistente en la rosácea.
Evidencia de ensayos clínicos para la brimonidina
La aprobación del gel tópico de brimonidina se basó en los datos recopilados de más de 550 pacientes inscritos en dos estudios clínicos de fase 3, cada uno de un mes de duración. Los resultados de ambos estudios mostraron que los adultos que usaron Mirvaso demostraron una mejora significativamente mayor en el enrojecimiento facial de la rosácea que vehículo gel. Además, también se realizó un estudio a largo plazo en 276 sujetos que usaron gel tópico de brimonidina durante un máximo de 12 meses.
Estudios de corta duración 1 y 2
- Ambos estudios fueron aleatorios, doble ciego, ensayos clínicos controlados por vehículo.
- Los ensayos incluyeron a 553 sujetos de 18 años o más con eritema facial de rosácea persistente moderado o grave.
- Los pacientes fueron tratados una vez al día durante 4 semanas con gel o vehículo tópico Mirvaso.
- En general, el 99% de los sujetos eran caucásicos y el 76% eran mujeres.
- Base la gravedad de la enfermedad se calificó mediante una evaluación del eritema clínico (CEA) de 5 puntos escala y una escala de autoevaluación del paciente (PSA) de 5 puntos, en la que los sujetos puntuaron "moderado" o "grave" en ambos escamas.
- los primario eficacia El criterio de valoración en ambos ensayos pivotales fue el éxito compuesto de 2 grados, definido como la proporción de sujetos con una mejora de 2 grados tanto en CEA como en PSA medidos a las 3, 6, 9 y 12 horas del día 29.
- Además del día 29, se evaluó la eficacia el día 15 y el día 1.
Los hallazgos clave de eficacia se resumen en la tabla y las figuras siguientes.
| Éxito* | Estudio 1 | Estudio 2 | ||
|---|---|---|---|---|
| Gel tópico Mirvaso® (N = 129) | Gel de vehículo (N = 131) | Gel tópico Mirvaso® (N = 148) | Gel de vehículo (N = 145) | |
| Hora 3 | 31% | 11% | 25% | 9% |
| Hora 6 | 30% | 10% | 25% | 9% |
| Hora 9 | 26% | 10% | 18% | 11% |
| Hora 12 | 23% | 9% | 22% | 10% |
* Mejora de 2 grados en CEA y mejora de 2 grados en la escala de PSA el día 29
Reacciones adversas en los estudios 1 y 2
Las reacciones adversas notificadas en 330 personas tratadas con gel de brimonidina tópico aplicado una vez al día durante 29 días se resumen en la siguiente tabla.
| Gel tópico Mirvaso® (N = 330) No. pacientes (%) | Vehículo en gel (N = 331) No. pacientes (%) | |
|---|---|---|
| Eritema | 12 (4%) | 3 (1%) |
| Enrojecimiento | 9 (3%) | 0 |
| Sensación de ardor en la piel | 5 (2%) | 2 (1%) |
| Dermatitis | 3 (1%) | 1 (<1%) |
| Parestesia (hormigueo / espinoso) | 2 (1%) | 1 (<1%) |
| Acné | 2 (1%) | 1 (<1%) |
| Visión borrosa | 2 (1%) | 0 |
| Congestión nasal | 2 (1%) | 0 |
Abierto estudio a largo plazo
- Se realizó un estudio de etiqueta abierta del gel tópico de brimonidina cuando se aplica una vez al día durante hasta un año en personas con eritema facial de rosácea persistente (no transitorio).
- A los pacientes se les permitió utilizar otras terapias para la rosácea.
- Un total de 276 sujetos aplicaron gel tópico de brimonidina durante al menos un año.
- Los más comunes eventos adversos reportados fueron rubor (10%), eritema (8%), aumento de rosácea (5%), nasofaringitis (5%), sensación de ardor en la piel (4%), aumento de la presión intraocular (4%) y dolor de cabeza (4%).