Anuncio
Cáncer de piel
Aplicación para facilitar el autoexamen de la piel y la detección temprana. Lee mas.
Introducción
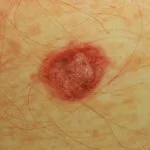
Melanoma es una forma de piel potencialmente grave cáncer. Algunos pacientes tienen melanoma avanzado con alto riesgo de reaparición, progresión y metástasis, a pesar de la cirugía para extirpar el primario tumor.
Intralesional /actual La terapia se puede utilizar para administrar la terapia directamente en una recurrencia o metástasis local. Los objetivos de la terapia intralesional son destruir el objetivo lesión y estimular regresión de otro, sin tratar lesiones induciendo una respuesta inmune al melanoma.
Se han investigado una variedad de agentes, incluidos varios citocinas (Mensajero proteinas), pequeño molécula inmunomoduladores y virus y plásmidos vectores expresando inmunológicamente activo moléculas.
¿Quiénes son los mejores candidatos para la terapia tópica o intralesional para el melanoma?
Los candidatos para la terapia de melanoma intralesional / tópico incluyen:
- Pacientes con irresecable, múltiples o avanzados a nivel local / regional metastásico Melanoma en estadio IIIb / co estadio IV M1a, con enfermedad a distancia o sin esta
- Tumores que son accesibles a la inyección directa
- Pacientes que no pueden tolerar otras terapias agresivas
Agentes efectivos para la inmunoterapia intralesional / tópica del melanoma
Bacillus Calmette-Guerin (BCG) fue el primer tratamiento intralesional descrito.
- Se informó que el uso inicial de BCG resultó en controlar en el 90% de los inyectados intradérmico metástasis e inducido sistémico respuesta inmune al melanoma antígenos.
- En otro estudio se ha informado de una tasa de respuesta del 17% para pacientes sometidos a inyección intralesional de BCG.
- El interés en BCG retrocedió cuando anafiláctico reacciones y muerte por diseminado Se informó BCG.
- Subsecuente aleatorizado los ensayos de BCG no confirmaron un beneficio clínico significativo y se interrumpió su uso.
Se han realizado más investigaciones sobre la terapia intralesional / tópica desde los ensayos de BCG, junto con una variedad de métodos de tratamiento, como:
- Dióxido de carbono láser
- Crioterapia
- Electroporación (ECT)
- Citotóxico agentes (cisplatino intralesional, 5-fluorouracilo tópico)
- Citocinas (intralesional interleucina [IL]-2 e interferón [IFN]-alpha y beta).
Se ha observado que la IL-2 produce tasas de respuesta general del 70% al 80% y respuestas completas del 62,5% al 69%, pero el tratamiento requiere mucho tiempo, es costoso y no ha demostrado la regresión de las lesiones no inyectadas.
Recientemente se ha incrementado el interés por tres agentes en investigación que parecen destruir tumores en el sitio de inyección y producir efectos sistémicos:
- OncoVEXGM-CSF
- Alovectina-7
- Rosa de Bengala (PV-10)
OncoVEXGM-CSF (T-VEC)
Inyección intralesional de granulocito macrófago factor estimulante de colonias (GM-CSF) en metástasis de melanoma da como resultado la infiltración de macrófagos y linfocitos en el tumor. El GM-CSF tiene una alta tasa de respuesta y ofrece esperanza de estimulación inmunológica regional y regresión de las lesiones no inyectadas.
OncoVEXGM-CSF, ahora llamado T-VEC (Talimogene laherparepvec), es un virus HSV-1 oncolítico modificado genéticamente para secretar el citocina GM-CSF. Los investigadores diseñaron T-VEC tomando herpes simplex virus tipo 1a (el virus del herpes labial) e introduciendo genético mutaciones para eliminar su capacidad de causar herpes y transformarlo en una terapia para matar el cáncer.
- Un ensayo clínico de fase I demostró una tasa de respuesta objetiva del 26% en lesiones inyectadas y no inyectadas (incluidas visceral depósitos).
- En un ensayo de fase 2, el 20 por ciento de los pacientes logró una respuesta completa y el 28 por ciento logró alguna tasa de respuesta objetiva (respuesta completa + respuesta parcial). El noventa y dos por ciento de las respuestas duraron al menos 6 meses. los mediana la supervivencia global fue de 23,3 meses en el grupo T-VEC y de 19,0 meses en el grupo de control.
Con base en estos resultados preliminares, actualmente se está llevando a cabo un ensayo clínico de fase 3 aleatorizado prospectivo internacional en pacientes con melanoma en estadio IIIB o IIIC o estadio IV (OPTiM) irresecable (2014).
- El ensayo de fase 3 OPTim ha inscrito a 436 pacientes con melanoma en estadio IIIB / IV asignados al azar 2: 1 a T-VEC versus subcutáneo GM-CSF solo.
- Los resultados provisionales del estudio OPTiM mostraron que el virus mejoró significativamente la tasa de respuesta duradera en comparación con GM-CSF solo en pacientes con metástasis de melanoma (16,3% frente a 2,1%; p <0,0001). Una respuesta duradera se definió como una respuesta completa o parcial que comenzó dentro de los 12 meses posteriores al inicio del tratamiento y duró 6 meses o más.
Alovectin-7®
La expresión del complejo mayor de histocompatibilidad de clase I (MHC-I) se reduce en las células de melanoma, lo que se cree que les permite evadir el reconocimiento por Células T. Los componentes de MHC-1 incluyen HLA-Microglobulina B7 y ß2.
Allovectin-7® es un plásmido HLA-B7 / beta2-microglobulina formulado con catiónico lípidos. Aumenta la capacidad del sistema inmunológico para reconocer las células cancerosas y matarlas. En 1999, la FDA de EE. UU. Otorgó la designación de fármaco huérfano alovectina-7 para el tratamiento intralesional de invasor y melanoma metastásico.
- En un ensayo de fase 2 de 133 pacientes con melanoma, la tasa de respuesta general fue del 12% sin toxicidad de grado 3 o superior.
- Un ensayo de fase 3 de 2 mg de Allovectin-7® intralesional en pacientes con melanoma en estadio III o IV no demostró una mejora estadísticamente significativa en la tasa de respuesta objetiva a las 24 semanas o más o en la supervivencia general, en comparación con dacarbazina o temozolomida.
PV-10 (10% p / v Rosa de Bengala en salina)
El disódico de rosa de Bengala (RB) es un derivado de fluoresceína de molécula pequeña que se ha utilizado en ensayos radiomarcados para hepático función (RB hepático radiomarcado con 131I). También se utiliza como colorante en gotas para los ojos, ya que tiñe las células conjuntivales dañadas.
También se pueden usar inyecciones de RB al diez por ciento (p / v) en solución salina (PV-10) para destruir localizado tumores como el melanoma metastásico. RB se acumula en el lisosomas de células cancerosas, que se someten a autofagia en 30-60 minutos. Luego, los fragmentos de tumor se exponen a antígeno-que presentan células, lo que resulta en un aumento de células T en periférico sangre, incluidas las células CD3 + y CD8 + citotóxicas, un inmunológico respuesta antitumoral.
Estudio de fase 1
- A 11 pacientes con melanoma metastásico en estadio III se les inyectó PV-10 a una dosis de 0,5 ml / cc de volumen de lesión. El tratamiento fue bien tolerado y se observó una respuesta objetiva en 12/26 lesiones diana.
- Se observaron otras 28 lesiones no tratadas por un posible efecto de espectador. Estos tuvieron una tasa de respuesta objetiva del 27% que aumentó al 44% en pacientes que tuvieron una respuesta positiva de las lesiones diana.
Estudio de fase 2
- En un ensayo internacional multicéntrico en 80 pacientes con melanoma medible en estadio III-IV, se administraron hasta 4 inyecciones intralesionales de PV-10 a intervalos mensuales durante un período de 16 semanas, con una dosis mediana de PV-10 por tratamiento de 1,6 mL.
- El veinticuatro por ciento de los pacientes tuvo respuestas completas (RC) de las lesiones objetivo y el 25 por ciento tuvo respuestas parciales (PR).
- Entre los 38 sujetos con lesiones de los espectadores, se informó que la RC de sus lesiones no tratadas fue del 24 por ciento. La regresión de las lesiones de los espectadores se correlacionó fuertemente con una respuesta en las lesiones objetivo.
- En un análisis adicional de los primeros 40 pacientes, aquellos con RC lograron una supervivencia libre de progresión significativamente más larga (11,1 meses) que aquellos con enfermedad estable o progresivo enfermedad (2,8 y 2,7 meses, respectivamente).
Estudio de fase 3
- Un ensayo de fase 3 de PV-10 está en curso (2014) y se espera que inscriba hasta 300 sujetos con melanoma en estadio IIIB-IIIC.
- En este ensayo, PV-10 se comparará con un grupo de control de quimioterapia con dacarbazina (DTIC) o temozolomida, con la supervivencia libre de progresión como criterio de valoración principal.
Difenciprona
Difenciprona (DPCP) es un sensibilizador de contacto con inmunomodulador efectos, comúnmente utilizados para alopecia areata y verrugas virales.
Informes recientes indican que la difenciprona tópica (DPCP) puede ser eficaz en tránsito y cutáneo melanoma metastásico solo y en combinación con cimetidina o dacarbazina y radioterapia. Se presume que la difenciprona actúa promoviendo linfocito-destrucción tumoral mediada, aunque se desconoce su mecanismo de acción exacto.
- En un estudio australiano, 50 pacientes con melanoma fueron tratados con DPCP solo durante al menos 1 mes. DPCP diluido en agua crema se aplicó a las lesiones de melanoma a intervalos semanales, 10 a 14 días después de la sensibilización.
- Se observó una eliminación completa de la enfermedad cutánea en el 46% y una respuesta parcial en otro 38% de los pacientes. los media La duración del tratamiento con DPCP hasta la eliminación de todas las lesiones cutáneas fue de 8 meses. La duración media de la respuesta completa fue de 17 meses.
El imiquimod, modificador tópico de la respuesta inmune, se puede agregar a DPCP en refractario casos. Imiquimod tiene antivírico y antitumorales TH1, mediados a través de la activación de Toll-like receptor 7 y TLR 8 y la secreción de varias citocinas que incluyen interferón, IL-1, IL-6, IL-8, IL-10 e IL-12. Anteriormente se ha utilizado sin autorización para tratar el melanoma. en el lugar y melanoma metastásico cutáneo.