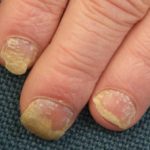
Introducción
Apremilast (Otezla®; Cellgene, Nueva Jersey, EE. UU.) Es un pequeñomolécula inhibidor del enzima fosfodiesterasa 4, que juega un papel importante en crónico inflamación asociado con la psoriasis.
El 23 de septiembre de 2014, la Administración de Alimentos y Medicamentos de los EE. UU. (FDA) aprobó apremilast para el tratamiento de pacientes con placa psoriasis principalmente sobre la base de los resultados de 2 ensayos clínicos multicéntricos: ESTEEM 1 y ESTEEM 2.
En julio de 2019, la FDA también aprobó el apremilast para el tratamiento de úlceras asociado con la enfermedad de Behçet.
Ensayos ESTEEM
- La aprobación de la FDA para la psoriasis en placas de moderada a grave se basó en los resultados de los ensayos ESTEEM.
- En estos ensayos, 1257 pacientes con psoriasis en placas de moderada a grave fueron aleatorizados 2: 1 a apremilast 30 mg dos veces al día (después de un período de ajuste de dosis) o placebo.
- los primario El criterio de valoración fue el número de pacientes con una mejora del 75% en el índice de gravedad y área de psoriasis (PASI-75).
- En ESTEEM 1, un número significativamente mayor de pacientes que recibieron apremilast lograron una reducción del 75% en la puntuación PASI (índice de gravedad del área de psoriasis, una herramienta utilizada para medir la gravedad y extensión de la psoriasis) en comparación con placebo (33,1% frente a 5,3%; p <0,0001) a las 16 semanas.
- En ESTEEM 2, significativamente más pacientes que recibieron apremilast también alcanzaron PASI-75 en comparación con placebo (28,8% frente a 5,8%; P <0,0001) a las 16 semanas.
- En los ensayos ESTEEM, la mayoría de eventos adversos con apremilast se consideraron de gravedad leve a moderada y consistieron principalmente en náuseas y vómitos, que generalmente se resolvieron en un mes.
- En particular, los ensayos clínicos clave con Enbrel® (etanercept) han encontrado que aproximadamente del 38% al 40% de los pacientes logran PASI-75 en un período de tiempo similar. Los ensayos clave con Remicade® (infliximab) y Humira® (adalimumab) han encontrado que aproximadamente del 60% al 64% y del 49% al 59%, respectivamente, logran PASI-75 en un período de tiempo similar.
La proporción de sujetos que lograron respuestas PASI-75 y sPGA (puntuación de evaluación global del médico estática – impresión del médico de la enfermedad en un solo punto) de clara (0) o casi clara (1), se presentan en la Tabla 1.
| ESTIMA – 1 | ESTIMA 2 | |||
|---|---|---|---|---|
| Placebo | Apremilast | Placebo | Apremilast | |
| No. aleatorizado | 282 | 562 | 137 | 274 |
| PASI 75%; No. (%) | 15 (5,3) | 186 (33,1) | 8 (5,8) | 79 (28,8) |
| sPGA no. (%) | 11 (3,9) | 122 (21,7) | 6 (4,4) | 56 (20,4) |
Reacciones adversas
- La seguridad de apremilast se ha evaluado en 3 pacientes doble ciego, ensayos controlados con placebo en los que participaron 1426 sujetos adultos con psoriasis en placas de moderada a grave.
- Los sujetos fueron asignados al azar a 30 mg dos veces al día de apremilast o placebo.
- Los sujetos tenían edades comprendidas entre 18 y 83 años, con un mediana edad de 46 años.
- Las reacciones adversas se resumen en la Tabla 2.
Tabla 2 Reacciones adversas notificadas en> 1% de los sujetos tratados con apremilast y con mayor frecuencia que en los sujetos tratados con placebo; hasta el día 112 (semana 16)
| Reacción adversa | Placebo (N = 506) núm. (%) | Apremilast (N = 920) núm. (%) |
|---|---|---|
| Diarrea | 32 (6) | 160 (17) |
| Náusea | 35 (7) | 155 (17) |
| Tracto respiratorio superior infección | 31 (6) | 84 (9) |
| Cefalea tensional | 21 (4) | 75 (8) |
| Dolor de cabeza | 19 (4) | 55 (6) |
| Dolor abdominal | 11 (2) | 39 (4) |
| Vómitos | 8 (2) | 35 (4) |
| Fatiga | 9 (2) | 29 (3) |
| Dispepsia | 6 (1) | 29 (3) |
| Disminuir el apetito. | 5 (1) | 26 (3) |
| Insomnio | 4 (1) | 21 (2) |
| Dolor de espalda | 4 (1) | 20 (2) |
| Migraña | 5 (1) | 19 (2) |
| Evacuaciones intestinales frecuentes | 1 (0) | 17 (2) |
| Depresión | 2 (0) | 12 (1) |
| Bronquitis | 2 (0) | 12 (1) |
| Diente absceso | 0 (0) | 10 (1) |
| Foliculitis | 0 (0) | 9 (1) |
| Seno dolor de cabeza | 0 (0) | 9 (1) |
Direcciones futuras
- Apremilast ha demostrado seguridad y eficacia en el tratamiento de psoriásicos artritis y psoriasis en placas.
- Sin embargo, apremilast no se ha comparado con otros tratamientos aprobados para la psoriasis y los resultados de los ensayos controlados con placebo sugieren un grado de eficacia que puede ser menor que la mayoría de las alternativas biológicas aprobadas por la FDA.
- Es probable que apremilast ofrezca una alternativa oral a los biológicos en pacientes que no responden adecuadamente a los biológicos (p. Ej., Adalimumab, infliximab, etanercept, ustekinumab), aquellos con una respuesta disminuida con el tiempo y aquellos que no pueden tomar o tolerar los agentes biológicos.
- Se necesitan más datos de ensayos clínicos y experiencia del mundo real para evaluar el verdadero valor de apremilast frente a otros agentes en el tratamiento de la psoriasis.