Introducción
En diciembre de 2016, la Administración de Drogas y Alimentos de los EE. UU. (FDA) aprobó el crisaborol actual ungüento, 2%, para tratar de leve a moderada atópico dermatitis en pacientes de 2 años de edad y mayores. Es una fosfodiesterasa a base de boro 4 inhibidor (PDE-4) y se comercializará como EUCRISA ™. Fue desarrollado por Anacor Pharmaceuticals Inc. (Palo Alto, California, EE. UU.), Que Pfizer Inc (Nueva York, EE. UU.) Adquirió en mayo de 2016.
El crisaborol es una monoterapia tópica no esteroidea que inhibe la fosfodiesterasa (PDE) -4 enzima en la piel. Se ha demostrado que la PDE-4 hiperactiva contribuye a los signos y síntomas de la dermatitis atópica.
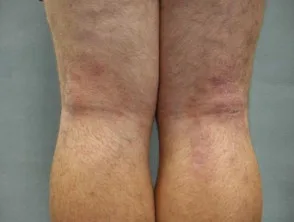
Dermatitis atópica
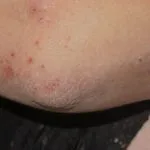
Dermatitis atópica del cuello
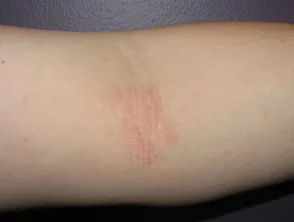
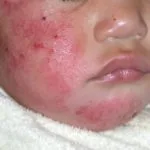
Dermatitis atópica
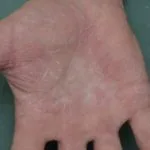
Dermatitis atópica
¿Cómo actúa el crisaborol?
- El mecanismo o mecanismos específicos por los que el crisaborol ejerce su terapéutico la acción no está bien definida.
- La dermatitis atópica se caracteriza por células auxiliares T (Th2) de tipo 2 inflamación.
- El crisaborol es un inhibidor de la enzima PDE-4.
- PDE-4 inhibición resulta en un aumento intracelular Niveles de monofosfato de adenosina cíclico (cAMP).
- El crisaborol modifica la inflamación en la dermatitis atópica al inhibir la degradación del AMPc por la PDE4, lo que resulta en una modificación posterior de nuclear factor-kB y Célula T vías de señalización.
Dosificación y administración
- El crisaborol es solo para uso tópico y no para uso oftálmico, oral o intravaginal utilizar.
- Se aplica como una capa fina sobre el área o áreas afectadas dos veces al día.
- Los ingredientes inactivos en la pomada incluyen vaselina blanca, propilenglicol, mono y diglicéridos, parafina, hidroxitolueno butilado y edetato cálcico disódico.
Uso en poblaciones específicas
El embarazo
- No hay datos disponibles sobre el uso de crisaborol en mujeres embarazadas para informar sobre el riesgo asociado al fármaco de defectos de nacimiento importantes y aborto espontáneo.
- No adverso de desarrollo Se observaron efectos en conejas preñadas con la administración oral de crisaborol.
- Consulte la página de DermNet NZ sobre la seguridad de los medicamentos que se toman durante el embarazo.
Lactancia
- No existe información sobre la presencia de crisaborol en la leche materna o los efectos del fármaco en el lactante después de la aplicación tópica en mujeres que están amamantando.
- El crisaborol se absorbe sistémicamente.
- Se debe considerar el potencial riesgo-beneficio al prescribir crisaborol a la madre.
- Consulte la página de DermNet NZ sobre la lactancia y la piel.
Pediátrico utilizar
- Se ha establecido la seguridad y eficacia del crisaborol en pacientes pediátricos de 2 años en adelante.
- No se ha establecido la seguridad y eficacia del crisaborol en niños menores de 2 años.
Uso geriátrico
- Los estudios clínicos de crisaborol no incluyeron un número suficiente de sujetos de 65 años o más para determinar si responden de manera diferente a los sujetos más jóvenes.
¿Cuáles son los posibles efectos adversos del crisaborol?
- El efecto secundario más común del crisaborol es el dolor en el lugar de aplicación, como ardor o escozor.
- El crisaborol puede causar hipersensibilidad reacciones en el lugar de aplicación o en un lugar distante.
- Estos pueden ser graves y pueden incluir urticaria (póngase en contacto con urticaria), picazón, hinchazón y eritema.
- Si se presentan signos y síntomas de hipersensibilidad, se debe suspender el crisaborol inmediatamente e iniciar la terapia adecuada.
- Crisaborole es contraindicado en pacientes con hipersensibilidad conocida al crisaborol o cualquier componente del formulación.
El crisaborol es prometedor para la dermatitis atópica en estudios de fase 3
- El crisaborol es el primer antiinflamatorio tópico no esteroideo de su clase.inflamatorio, Inhibidor de la PDE aprobado para el tratamiento de la dermatitis atópica leve a moderada.
- El crisaborol representa un tratamiento tópico no esteroideo prometedor para mejorar el tratamiento de la dermatitis atópica.
- Mejora significativa en la gravedad de la enfermedad, prurito intensidad, y todos los demás signos y síntomas evaluados de la dermatitis atópica indican que el crisaborol puede apuntar al Patogénesis de la enfermedad.
- La novedosa química del boro del crisaborol permite síntesis de un bajomolecular-compuesto de peso (251 d) que facilita la penetración efectiva a través de la piel humana.
¿Crisbarole ayuda a otras afecciones de la piel?
Se ha informado que el crisaborol es beneficioso en intertriginoso/flexión psoriasis y psoriasis facial.