Wat is genetisch test voor melanoma?
genen dragen informatie in de vorm van DNA Y controleren hoe cellen werken EEN kiem lijn mutatie Het beïnvloedt elke cel in het lichaam. EEN somatisch mutatie is beperkt tot a tumor cel, zoals een melanoomcel.
Germline genetische tests voor melanoom geven informatie over de vraag of de patiënt een mutatie heeft die hem vatbaar maakt voor ontwikkelen melanoma.
- Ongeveer 10% van melanomen zijn secundair aan gen mutaties.
- De overige 90% van melanomen zijn sporadisch (niet gerelateerd aan genetische mutaties).
Als de patiënt drager is van een melanoomkiemlijngenmutatie, kan deze een verhoogd risico hebben op ontwikkelen een melanoom. Ze kunnen een positieve familiegeschiedenis van melanoom hebben en melanoom kan op jongere leeftijd verschijnen in vergelijking met sporadisch melanoom.
EEN biopsie melanoommonster kan in het laboratorium worden geanalyseerd somatische mutaties om informatie te geven over behandelingsmogelijkheden of voorspelling.
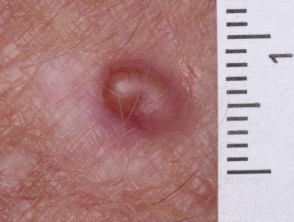
Melanoma
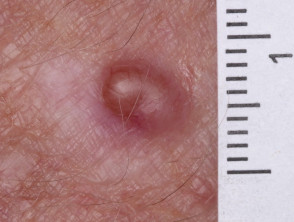
Amelanotische melanoommacro
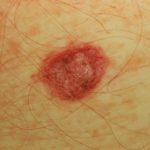
Groot melanoom in situ
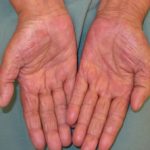
Lentigo maligna melanoom van 0,8 mm
Wat zijn de mutaties in het kiemlijngen van het melanoom?
Enkele van de kiembaangenmutaties die betrokken zijn bij huid melanoom omvat, maar is niet beperkt tot [1]:
- cyclineafhankelijk kinase remmer 2A-gen (CDKN2A)
- Cycline-afhankelijk kinase 4-gen (CDK4)
- Retinoblastoma-gen (RB1)
- TERT promotorgen, geassocieerd met microftalmie transcriptie factor genMITF) E318K
- BRCA1 geassocieerd eiwit 1 genBAP1)
- Microphthalmia-geassocieerde transcriptiefactor (MITF)
- tyrosinase (TYR) en tyrosinase-gerelateerd eiwit 1 (TYRP1)
- Interferon-regulerende factor 4-gen.
Kenmerken van cutane melanoomtumorsyndromen kunnen zijn:
- Vroeg begin van melanoom
- Meerdere primair melanomen
- Leden van één kant van de familie die ook een melanoom hebben gehad
- Een familiale neiging om andere zeldzame maligniteiten te ontwikkelen. [2].
CDKN2A-mutatie
CDKN2A Er is een mutatie gevonden in 1.2% van patiënten met een enkelvoudig primair melanoom en in 2.9% van patiënten met meerdere primaire melanomen. dragers van CDKN2A mutatie ontwikkelt vaak op jonge leeftijd huidmelanoom, heeft een positieve familiegeschiedenis van melanoom en kan ook vatbaar zijn voor pancreas kanker [3].
De Amerikaanse Academie van DermatologieDe in 2019 gepubliceerde richtlijn beveelt aan dat de volgende patiënten zich kunnen verantwoorden CDKN2A genetische tests indien beschikbaar [2]:
- Een familiegeschiedenis van invasief huidmelanoom of alvleesklierkanker (3 of meer getroffen leden aan één kant van de familie)
- Drie of meer primaire invasieve huidmelanomen, waaronder één tumor met vroege aanvang (<45 años de edad).
BAP1-mutatie
BAP1 mutatie is erkend als een zeldzame oorzaak van erfgenaam melanoma. kiembaan mutaties van BAP1 is geassocieerd met:
- Een verhoogd risico op oogmelanoom
- atypisch Spitz-tumoren (ook bekend als melanocytisch Atypisch gemuteerd in BAP1 intradermaal tumoren [MBAIT's])
- Cutaan melanoom
- nier cel carcinoom
- mesothelioom.
Ongeveer 13% kiembaandragers BAP1 De mutatie zal huidmelanoom ontwikkelen en een hoger percentage dragers zal oogmelanoom ontwikkelen. [2,4].
De in 2019 gepubliceerde richtlijn van de American Academy of Dermatology beveelt aan dat het volgende verhaal dit kan rechtvaardigen BAP1 Genetische test [2]:
- Een of meer atypische Spitz-tumoren en een familiegeschiedenis van mesothelioom, meningeoom of oogmelanoom
- Twee of meer atypische Spitz-tumoren.
Vertel me meer over genetisch testen voor melanoom
Erfelijkheidsadviseurs en medisch genetici kunnen kiembaangenetisch onderzoek voor melanoom regelen. Tijdens een eerste erfelijkheidsadviesafspraak zal de persoonlijke en familiale geschiedenis van de patiënt zorgvuldig worden beoordeeld om hun risico's op erfelijke kanker in te schatten. De patiënt krijgt dan advies over de voor- en nadelen van het uitvoeren van de genetische test. De uiteindelijke beslissing om genetische tests uit te voeren voor kiembaanmutaties is een complexe beslissing op basis van familiegeschiedenis, kankerpatronen, wensen van patiënten en waargenomen risico's versus voordelen [2].
Welke somatisch genetische tests kunnen worden uitgevoerd op de melanoomtumor?
oncogeen somatische mutaties zoals BRAF, NRAS, c-KIT of PTEN kan worden getest door immunohistochemie of genomische technieken. Van deze mutaties BRAF het is de meest voorkomende, waargenomen bij 50 tot 70% van huidmelanomen. Informatie over een oncogene mutatie kan de arts helpen bij het kiezen van de beste behandeling voor melanoom in een gevorderd stadium, aangezien er gerichte therapieën zijn zoals BRAF-remmers voor tumoren die bepaalde herbergen BRAF mutaties. Oncogene mutatietesten worden aanbevolen bij patiënten met metastatisch ziekte of als er een mogelijkheid is om deel te nemen aan een relevante klinische studie [2].
Somatisch genetisch testen op een tumor kan ook uitkomst bieden voorspelling informatie. De meeste prognostische tests zijn nog in onderzoek.
- TERT Promotormutaties kunnen worden geëvalueerd om diagnostische en prognostische informatie te verkrijgen. [2].
- Het Gene Expression Profile (GEP), ook bekend als de 31-gen prognostische test, bestaat uit een panel van 31 genen (28 signatuurgenen plus 3 controlegenen). De GEP kan worden gebruikt om melanoom te classificeren in "hoog risico" en "laag risico" tumoren. Van patiënten met een hoog risico wordt voorspeld dat ze een verhoogd risico lopen op melanoom op afstand metastase [5].
Wat zijn de voordelen van kiembaangenetisch testen voor melanoom?
De voordelen voor een individu zijn onder meer het kennen van hun aanleg tot melanoom of een ander type kanker, afhankelijk van het geanalyseerde gen [1].
- Een positieve test voor melanoom geeft aan dat de huid van de patiënt moet worden gecontroleerd door een deskundige op het gebied van vroege diagnose van melanoom, wat fotografische bewaking van de huid van het hele lichaam kan omvatten. dermatoscopie.
- Een positieve test kan erop wijzen dat de patiënt moet worden onderzocht op andere kankers. Bijvoorbeeld een patiënt met CDKN2A de mutatie kan periodiek worden gescreend op alvleesklierkanker.
- Genetische testen leiden tot een beter begrip van melanoom door bepaalde genmutaties te correleren met melanoom fenotypes en identificatie van nieuwe medicijnen voor patiënten.
Wat zijn de nadelen van kiembaanonderzoek voor melanoom?
Een positieve test kan bij een patiënt zorgen baren over het persoonlijke en familiale risico op het ontwikkelen van kanker, en kan ook zorgen baren over het afsluiten van een ziektekosten- of levensverzekering.
Een negatieve test kan de patiënt een vals gevoel van veiligheid geven, waardoor melanoomsurveillance en bescherming tegen de zon afnemen. Daarom is het belangrijk om de patiënt te informeren dat ongeveer 90% van huidmelanomen sporadisch is en niet gerelateerd is aan genetische mutaties.