Cos'è ustekinumab?
Ustekinumab (nome commerciale STELARA ™) è un trattamento biologico usato per trattare la psoriasi da moderata a grave. è un essere umano monoclonale anticorpo che si contrappone interleuchina-12 (IL-12) e IL-23. Risposte da buone a eccellenti si osservano in più di due terzi dei pazienti con cronica targa psoriasi trattata con ustekinumab.
Ustekinumab ha dimostrato in piccoli studi di essere utile in altre forme di psoriasi, tra cui un psoriasi, psoriasi eritrodermica, molto diffuso pustolosa psoriasi e palmoplantare pustolosi. È anche usato per trattare la psoriasi. artrite e il morbo di Crohn.
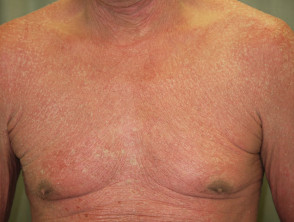
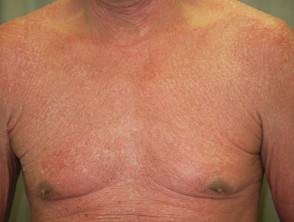
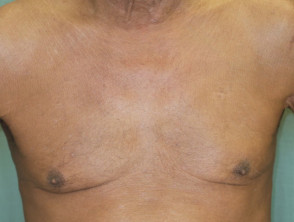
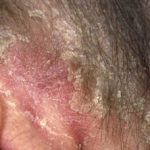
Psoriasi eritrodermica prima e 2 settimane dopo una singola dose di ustekinumab
Psoriasi eritrodermica prima di ustekinumab
Psoriasi eritrodermica 2 settimane dopo la prima dose di ustekinumab
Come funziona ustekinumab nella psoriasi?
La psoriasi è causata da un aumento della produzione di Cellule T. ed è influenzato da citochine, i messaggeri chimici prodotti dalle cellule. Alcune citochine fanno crescere rapidamente le cellule della pelle, producendo piatti dalla psoriasi. Ustekinumab è un anticorpo monoclonale che prende di mira la subunità p40 delle citochine IL-12 e IL-23, impedendo loro di legarsi e attivare T-linfociti.
Ustekinumab Dosaggio
Ustekinumab è somministrato da sottocutaneo iniezione. La seconda dose viene somministrata 4 settimane dopo la prima iniezione e dosi aggiuntive vengono somministrate ogni 12 settimane. Raggiunge il suo massimo effetto intorno alle 28 settimane.
- La dose per i pazienti di peso inferiore a 100 kg è di 45 mg.
- La dose per i pazienti che pesano più di 100 kg è di 90 mg.
- Ogni iniezione è meglio somministrata in un punto diverso (come la parte superiore delle braccia, i glutei, le cosce o l'addome)
Eventi avversi a causa di ustekinumab
Ad oggi, avverso infezioni Sono coerenti con quanto visto con altri farmaci biologici.
- Infezioni: Ustekinumab può aumentare il rischio di infezioni e riattivazione di latente gravi infezioni batterica, infezioni fungine e virali sono state osservate nei soggetti trattati con il farmaco.
- Neoplasie: ustekinumab è un immunosoppressore e può aumentare il rischio di malignità (Cancro) compresi i tumori della pelle.
- Sono stati segnalati disturbi del sistema immunitario durante l'uso post-approvazione con ustekinumab. Questi hanno incluso gravi reazioni allergiche (anche angioedema, mancanza di respiro e bassa pressione sanguigna) e ipersensibilità (allergia) reazioni (incluso eruzione e orticaria).
- Le reazioni al sito di iniezione includono dolore, gonfiore, prurito, ispessimento, sanguinamento e lividi.
Precauzioni quando si considera ustekinumab
- Cronico infezione o una storia di ricorrente infezione. Ustekinumab non deve essere somministrato fino a quando l'infezione non viene risolta o adeguatamente trattata.
- I pazienti trattati con ustekinumab possono esserlo suscettibile alle infezioni (tra cui tubercolosi, atipico micobatteri), salmonella (compresi i ceppi non tifoidi) e Bacillus Calmette-Guerin (BCG).
- Ustekinumab non deve essere somministrato a pazienti con tubercolosi attiva. Prima del trattamento biologico, devono essere eseguiti radiografie del torace, test di Mantoux indiretti e/o QuantiFERON gold. Considerare il trattamento antitubercolare prima di iniziare ustekinumab nei pazienti con una storia di tubercolosi latente o attiva. I pazienti trattati con ustekinumab devono essere attentamente monitorati per segni e sintomi di tubercolosi attiva durante e dopo il trattamento.
Vaccini e ustekinumab
Lo stato di immunizzazione deve essere rivisto prima di iniziare ustekinumab. Se necessario, le vaccinazioni devono essere aggiornate prima del trattamento con un agente biologico. Si raccomanda la vaccinazione antinfluenzale annuale.
Poiché possono indurre malattia in soggetti immunocompromessi, i vaccini vivi non devono essere utilizzati durante il trattamento con ustekinumab. I vaccini virali vivi attenuati attualmente disponibili includono morbillo, parotite, rosolia, varicella, giallo febbre, influenza (vaccino intranasale) e vaccino antipolio orale. I vaccini batterici vivi attenuati includono BCG e vaccino contro il tifo orale.
Maggiori informazioni sull'immunizzazione su immunosoppressi dermatologia pazienti.
Interazioni farmacologiche con Ustekinumab
- Non sono stati condotti studi formali di interazione farmacologica con ustekinumab.
- La sicurezza di ustekinumab in combinazione con immunosoppressore agenti o fototerapia non è stata valutata.
Uso di ustekinumab in popolazioni specifiche
Categoria di gravidanza B
Non ci sono studi su ustekinumab nelle donne in gravidanza. Ustekinumab deve essere usato durante la gravidanza solo se il potenziale beneficio giustifica il potenziale rischio per il feto.
Madri che allattano
Si deve usare cautela quando ustekinumab viene somministrato a una donna che allatta. Rischi sconosciuti per il bambino di origine gastrointestinale o sistemico L'esposizione a ustekinumab deve essere valutata rispetto ai noti benefici dell'allattamento al seno.
Pediatrico uso
Uno studio ha dimostrato che la sicurezza e l'efficacia di ustekinumab nei bambini di età compresa tra 12 e 17 anni è simile a quella degli adulti.
Epatica e renale disabilità
No farmacocinetica Sono disponibili dati in pazienti con malattia epatica o renale trattati con ustekinumab.
Monitoraggio durante l'assunzione di ustekinumab
Si raccomanda che i pazienti che assumono farmaci biologici eseguano esami del sangue di routine circa ogni 6 mesi, inclusi emocromo completo e test di funzionalità epatica. I test per la tubercolosi dovrebbero essere ripetuti di tanto in tanto.